
| A、FeO | B、Fe2O3 | C、FeCl3 | D、Fe2(SO4)3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(09全国卷Ⅱ29) (15分)现有A、B、C、D、E、F六种化合物,已知它们的阳离子有![]() ,
,![]() 阴离子有
阴离子有![]() ,现将它们分别配成
,现将它们分别配成![]() 的溶液,进行如下实验:
的溶液,进行如下实验:
① 测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 向D溶液中滴加![]() 溶液,无明显现象;
溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1) 实验②中反应的化学方程式是 ;
(2)E溶液是 ,判断依据是 ;
(3)写出下列四种化合物的化学式:A 、C 、D 、F .
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)现有A、B、C、D、E、五种化合物,已知它们的阳离子有K+、Ag+、Ba2+、Fe2+、Al3+阴离子有Cl-、OH-、NO3-、SO42-、CO32-,现将它们分别配成0.1mol·L-1的溶液,进行如下实验:
① 测得溶液A、C呈碱性,且碱性为A> C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④ 向E 溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1)实验④中反应的化学方程式是 。
(2)写出下列四种化合物的化学式:
A ,C D ,E 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省高三下学期第一次模拟考试化学试卷 题型:填空题
(13分)现有A、B、C、D、E、F六种化合物,已知它们的阳离子有 ,阴离子有
,阴离子有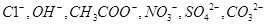 ,现将它们分别配成
,现将它们分别配成 的溶液,进行如下实验:
的溶液,进行如下实验:
① 
 测得溶液A、C、E呈碱性,且碱性为A>E>C;
测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 
 向D溶液中滴加
向D溶液中滴加 溶液,无明显现象;
溶液,无明显现象;
④ 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。

 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1) 实验②中反应的化学方程式是

 (2)E溶液是
,判断依据是
(2)E溶液是
,判断依据是
(3)写出下列四种化合物的化学式:A 、C
、
 D
、F
。
D
、F
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com