
����Ŀ�����ӹ�ҵ�ǹ���֧����ҵ֮һ��Ҳ�����˿�ѧ������չ��ҵ���������ӹ�ҵ������������Ϊ30%��FeCl3��Һ��ʴ����ͭ���ľ�Ե�壬�Ƴ�ӡˢ��·�壬������Ӧ�Ļ�ѧ����ʽΪ��2FeCl3+Cu�T2FeCl2+CuCl2 ��
��1�����鸯ʴ�����Һ���Ƿ���Fe3+ �� Ӧѡ�õ��Լ��� ��
��2��Ϊ�˴�ʹ�ù��ĸ�ʴ��Һ�л���ͭ���������Ƶô�����FeCl3��Һ��������ͼ��ʾʵ�鲽�裮���ڸ��ո��������ʵ��Ļ�ѧʽ��ʹʵ��ﵽԤ��Ŀ�ģ�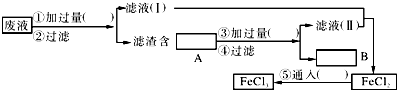
��3��д���йػ�ѧ��Ӧ�����ӷ���ʽ�� ��
���𰸡�
��1��KSCN��Һ
��2����ΪFe|��Ϊ����|��ΪCl2|AΪFe��Cu��BΪCu
��3��2Fe3++Fe�T3Fe2+ �� Fe+Cu2+�TFe2++Cu��Fe+2H+�TFe2++H2����2Fe2++Cl2�T2Fe3++2Cl��
���������⣺��1�����鸯ʴ�����Һ���Ƿ���Fe3+ �� Ӧѡ�õ��Լ���KSCN��Һ�����Դ��ǣ�KSCN��Һ����2��CuCl2��FeCl3�����۷�Ӧ����Fe2+��Cu����ҺI�к��Ȼ�������������A����Fe��Cu����ȥ���е�Feѡ�â�Ϊ�������ᣬ���˵õ���ҺII�к��Ȼ�������HCl��BΪCu�����Ȼ�������Һ��ͨ������������Ȼ��������ΪFe����Ϊ���ᣬ��ΪCl2 �� AΪFe��Cu��BΪCu�����Դ��ǣ���ΪFe����Ϊ�����ΪCl2��AΪFe��Cu��BΪCu����3���йػ�ѧ��Ӧ�����ӷ���ʽΪ2Fe3++Fe�T3Fe2+ �� Fe+Cu2+�TFe2++Cu��Fe+2H+�TFe2++H2����2Fe2++Cl2�T2Fe3++2Cl�� �� ���Դ��ǣ�2Fe3++Fe�T3Fe2+ �� Fe+Cu2+�TFe2++Cu��Fe+2H+�TFe2++H2����2Fe2++Cl2�T2Fe3++2Cl


 ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʣ��ٵ�ˮ����������Һ����NaOH��Һ����ϡ�����Ũ���ᡣ�ڽ��е��۵�ˮ��ʵ��(��������ˮ����Pˮ���Ƿ���ȫ)ʱ���������⣬����ʹ�������Լ�������һ���֣��ж�ʹ�õ��Լ������Ⱥ�˳��Ϊ( )
A.�ܢ٢ۢ�
B.�٢ܢڢ�
C.�ݢ٢ۢ�
D.�٢ݢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦN2O4(g) ![]() 2NO2(g) ��H>0��ƽ����ϵ��������
2NO2(g) ��H>0��ƽ����ϵ��������![]() �������ʵ���
�������ʵ���![]() ֮��M��M=
֮��M��M=![]() /
/![]() ���ڲ�ͬ�¶�����ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�
���ڲ�ͬ�¶�����ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ�
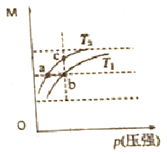
A. �¶ȣ�T1 ��T2
B. ƽ�ⳣ��K(a)=K(b)<K(c)
C. ��Ӧ���ʣ� ![]()
D. ��M=69g��mol-1 ʱ��n(NO2)��n(N2O4)=1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڴ�����������Һ�巴Ӧ������������ˮ��Ӧ���ü���Ҳ����Ҫ������ԭ����(����)
A.�������ǻ��Ӱ�죬�������ϵ���ԭ�ӻ����Բ���
B.�������ǻ��Ӱ�죬���ǻ��ϵ���ԭ�ӱ����
C.�ǻ�Ӱ���˱�����ʹ�����ϵ���ԭ�ӱ�û���
D.����Ӱ���ǻ���ʹ�ǻ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Iij�¶��£�Kw=10��12 ��
��1���������¶Ȳ��䣬������ˮ�м���g��NaOH���壬����ˮ��1L������ʹ��Һ�е��������H+��OH����Ũ�ȳ˻�����c��H+��c��OH����=10��22
��2���������¶Ȳ��䣬ij��Һ��c��H+��Ϊ1��10��7mol/L�������Һ���ԣ�ѡ��ᡱ��������С���
��3����֪������Kw[Fe��OH��3]=4.0��10��38 �� ��FeCl3��Һ�м���NaHCO3��Һ��������Ӧ�����ӷ���ʽΪ �� ����������Һ��pH����Ϊ4������Һ��Fe3+��Ũ��Ϊmol/L��
��4��������ƽ���ƶ�ԭ������������ʵ��
FeS������ˮ����������ϡ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ��ǿ�ᣬ�����Ũ�ȳ���40%�ͻ�Ѹ�ٷֽ⣬��Ӧ�Ļ�ѧ����ʽΪ��8HClO3�T3O2��+2Cl2��+4HClO4+2H2O�����������������С�⣺
���������仯�����У�������ԭ��Ӧ�Ĺ����������ѧʽ����
�ڸ÷�Ӧ���������������ѧʽ���������û�������ƽ����Է������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ�����ԼΪ6.02��1023 mol��1��NA��������˵����ȷ���ǣ� ��
A.���³�ѹ�£�16g O2��16g O3������ԭ��������NA
B.���ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl������Ϊ NA
C.��״���£�2.24LCCl4����ԭ����Ϊ0.5NA
D.��״���£�22.4 L���������е�������ĿԼΪ4��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�̿����е�ⱥ��ʳ��ˮ��ʵ��װ�ã��ݴˣ�������������ȷ���ǣ� �� 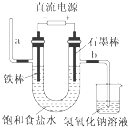
A.װ���У�a���ܲ�������
B.��ʯī���缫������NaOH����
C.b�ܵ�����������
D.��ʳ��ˮΪ����ԭ����ȡ�����Ȳ�Ʒ�Ĺ�ҵ��Ϊ���ȼҵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
2H2��g��+O2��g���T2H2O��l����H=��571.6kJmol��1��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=��890kJmol��1 ��
����H2��CH4�Ļ������112L����״������ʹ����ȫȼ������CO2��H2O��l������ʵ���÷�Ӧ����3695kJ����ԭ���������H2��CH4�����ʵ���֮���ǣ� ��
A.1��1
B.1��3
C.1��4
D.2��3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com