
【题目】容量瓶的瓶壁上未标明的是( )
A.刻度线
B.温度
C.浓度
D.容积
科目:高中化学 来源: 题型:
【题目】下列除去杂质的操作方法不正确的是( )
A.镁粉中含少量铝粉:加足量氢氧化钠溶液充分搅拌后过滤
B.碳酸钠溶液中含少量碳酸氢钠:加足量澄清石灰水
C.自来水中含少量Fe3+:蒸馏
D.硝酸钾固体中含少量氯化钾:配制80℃的饱和溶液,冷却、结晶、过滤、洗涤干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为 ,下列说法不正确的是( )
,下列说法不正确的是( )
A. X的化学式为C8H8
B. 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C. X能使高锰酸钾酸性溶液褪色
D. X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属单质跟一定浓度的硝酸反应,生成硝酸盐和氮氧化物等物质,假定只生成单一的还原产物,当参加反应的单质与被还原的硝酸的物质的量比为2:1时,还原产物可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)是火箭推进器中常用的高能燃料,已知0.4 mol液态肼和足量H2O2反应,生成N2和水蒸气,放出256. 65kJ的热量,请写出该反应的热化学方程式:__________。
(2)工业上制氢气的一个重要反应是:CO(g) +H2O(g)=CO2(g)+H2(g)
已知在25℃时:C(石墨)+![]() O2(g)=CO(g) △H1=-111kJ·mol-1
O2(g)=CO(g) △H1=-111kJ·mol-1
H2(g)+![]() O2(g)=H2O(g) △H2=-242 kJ·mol-1
O2(g)=H2O(g) △H2=-242 kJ·mol-1
C(石墨)+O2(g)=CO2(g) △H3=-394kJ·mol-1
试计算25℃时一氧化碳与水作用转化为氢气和二氧化碳反应的反应热△H=______kJ·mol-1
(3)CO2再在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与NaCO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol / L ,则生成沉淀所需CaCl2溶液的最小浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有①0.2 mol·L-1NaOH溶液和②0.2 mol·L-1HX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X-)。则:
(1)①中由水电离出的c(OH-)__________②中由水电离出的c(H+)(填“>”、“=”或“<”)。
(2)上述混合液中共存在__________种粒子。其中:c(HX)+c(X-)__________0.1 mol·L-1(忽略混合前后溶液体积变化;填“>”、“=”或“<”)。请根据电荷守恒写出一个用离子浓度表示的等式:_____________________________________。
(3)上述混合液显__________性(填“酸”、“碱”或“中”),其原因用离子方程式表示为_______________________________________。
Ⅱ.海水中含有大量的元素,常量元素(如氯)、微量元素(如碘)在海水中均以化合态存在。在25 ℃时,向0.1 mol·L-1的NaCl溶液中逐滴加入适量的0.1 mol·L-1硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1 mol·L-1的NaI溶液,看到的现象是___________________________,产生该现象的原因是(用离子方程式表示)__________________。
[已知25 ℃时Ksp(AgCl)=1.0×10-10、Ksp(AgI)=1.5×10-16]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是重要的无机化工原料,海藻灰化法是我国目前制碘的主要方法。某研究性学习小组查阅文献,设计并进行了以下模拟实验。
(已知:氯水中含有CL2分子,Cl2 +2I- = 2Cl- + I2)
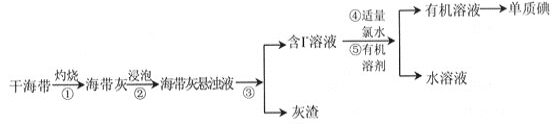
请回答:
(1)步骤①中灼烧海带用到的实验仪器是_____________(填序号)。
a. 试管 b. 坩埚 c. 烧杯 d.蒸发皿
(2)步骤③的实验操作是_______________________。
(3)步骤⑤实验操作可分解为如下几步:
(A)检验分液漏斗活塞和上口的玻璃塞是否漏水
(B)把50毫升碘水和15毫升CCl4加入分液漏斗中,并盖好玻璃塞
(C)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把漏斗放正
(D)把盛有溶液的分液漏斗放在铁架台的铁圈中
(E)静置,分层
(F)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔
(G)旋开活塞,用烧杯接收溶液
(H)从分液漏斗上口倒出上层水溶液
①上述(G)步骤的操作目的是____________________________________。
②能选用CCl4从碘水中萃取碘的原因是___________________________。
③以下物质中,能用来代替CCl4的是_______。
A汽油 B 酒精 C NaCl溶液 D NaOH溶液
(4)同学们观察到完成步骤⑤后,所得到的水溶液呈淡黄色。某同学推断其中可能含有碘单质,检验方法是: _______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】147 g H2SO4的物质的量是______;0.5 mol H2SO4的质量是______;其中含有_____mol H,含有_____mol O;2 mol H2SO4 中含有H2SO4分子数为______个,含有氢原子数为_______个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,发生3A+B = 2C (均为气体)的反应,若最初加入A和B都是4mol, A的平均反应速率是0.12mol/(L.s),则10s后容器中的B的物质的量是
A、1.6mol B、3.2mol C、3.6mol D、2.8mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com