
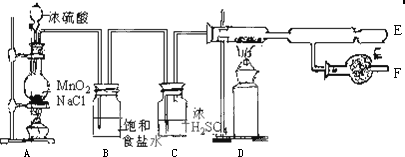
���� �ڼ��������£�Ũ������Ȼ��Ʒ�Ӧ����HCl��Ũ����Ͷ��������ڼ�������������Cl2��Ũ������лӷ��ԣ��������ɵ�Cl2�к���HCl��HCl��������ˮ�����͵�NaCl��Һ�����������ܽ⣬����B�������dz�ȥ�����е�HCl��Ϊ��ֹ�Ȼ����ڳ�ʪ�Ŀ����б�ը����Cװ�ø����������ڼ��������£�Al��������Ӧ����AlCl3�����ɵ��Ȼ�����E����ȴ�õ������Ȼ�����FĿ���Ǹ����������ֹ�Ȼ���Ҳˮ������϶���ը��
��1�������ƿ���Ȳ�����ը�ѣ�
��2��Aװ���з�������Ũ������Ȼ��Ƶķ�Ӧ��Ũ����Ͷ������̵ķ�Ӧ��
��3����ˮ�Ȼ����ǰ�ɫ���壬��178��������
��4��װ����ˮ�Ȼ������Լ�ƿ���ó�ʪ�����У����Զ���ը�����������������Ҽ���������������������Ӧ��������ը��
��5��Fװ��������δ��Ӧ����������Ҳ�ܸ��������
��6����ˮ�Ȼ����ڳ�ʪ�����У����������������˵���Ȼ���ˮ����������������HCl��
��� �⣺�ڼ��������£�Ũ������Ȼ��Ʒ�Ӧ����HCl��Ũ����Ͷ��������ڼ�������������Cl2��Ũ������лӷ��ԣ��������ɵ�Cl2�к���HCl��HCl��������ˮ�����͵�NaCl��Һ�����������ܽ⣬����B�������dz�ȥ�����е�HCl��Ϊ��ֹ�Ȼ����ڳ�ʪ�Ŀ����б�ը����Cװ�ø����������ڼ��������£�Al��������Ӧ����AlCl3�����ɵ��Ȼ�����E����ȴ�õ������Ȼ�����FĿ���Ǹ����������ֹ�Ȼ���Ҳˮ������϶���ը��
��1�������ƿ���Ȳ�����ը�ѣ�Ϊ��ֹ��ƿը�ѣ����Բ��ܲ����ȵ�ȼAװ�õľƾ��ƣ����Һ©���Ļ�����������Ũ����ע����ƿ��ʴ�Ϊ����ֹ��ƿ���Ȳ��������ѣ�
��2��Aװ���з�������Ũ������Ȼ��Ƶķ�Ӧ��Ũ����Ͷ������̵ķ�Ӧ����Ӧ����ʽΪH2SO4��Ũ���ᣩ+2NaCl$\frac{\underline{\;\;��\;\;}}{\;}$Na2SO4+2HCl��4HCl��Ũ���ᣩ+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$Cl2��+MnCl2+2H2O��
�ʴ�Ϊ��H2SO4��Ũ���ᣩ+2NaCl$\frac{\underline{\;\;��\;\;}}{\;}$Na2SO4+2HCl��4HCl��Ũ���ᣩ+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$Cl2��+MnCl2+2H2O��
��3����ˮ�Ȼ����ǰ�ɫ���壬��178������������D�����ɵ��Ȼ���������������E����ȴ�õ��Ȼ������壬�ʴ�Ϊ�����ɵ�AlCl3������������E������������
��4��װ����ˮ�Ȼ������Լ�ƿ���ó�ʪ�����У����Զ���ը�����������������Ҽ���������������������Ӧ��������ը�����������Aװ�õ�����������������B��Cװ�ö�ֱ�ӽ���D�ܣ�����ʵ����������ĺ����δ����ȥ��HCl���塢ˮ������Cl2һͬ����D�ܣ�������Ӧ����H2������H2��Cl2��ϱ�ը��H2O������ʹAlCl3��ˮˮ���ը�ȣ�
�ʴ�Ϊ��δ����ȥ��HCl���塢ˮ������Cl2һͬ����D�ܣ�������Ӧ����H2������H2��Cl2��ϱ�ը��H2O������ʹAlCl3��ˮˮ���ը�ȣ�
��5��Fװ��������δ��Ӧ����������ֹ��Ⱦ��������Ҳ�ܸ����������ֹ������ˮ��������D�ܣ�ʹ���ɵ�AlCl3�ܳ���
�ʴ�Ϊ�����ն����������������Ⱦ��������������ã���ֹ������ˮ��������D�ܣ�ʹ���ɵ�AlCl3�ܳ���
��6����ˮ�Ȼ����ڳ�ʪ�����У����������������˵���Ȼ���ˮ����������������HCl����Ӧ����ʽΪAlCl3+3H2O=Al��OH��3+3HCl�����ʴ�Ϊ��AlCl3+3H2O=Al��OH��3+3HCl����
���� ���⿼���Ʊ�ʵ�鷽����ƣ�Ϊ��Ƶ���㣬���ؿ���ѧ����ȡ��Ϣ����ѧ��������ȷ��ȡ��Ϣ�˽��Ȼ��������ص㼰ʵ��������������ǽⱾ��ؼ���֪������װ�����ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ӧ���ʼӿ죬ƽ�ⳣ��Ҳ����֮�仯 | |
| B�� | ����D��������ѧƽ�������ƶ� | |
| C�� | ����A������B��ת������� | |
| D�� | ƽ�ⳣ���ı���ʽΪK=$\frac{c��C��•c��D��}{c��A��^{2}•c��B��}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| T/�� | 25 | 80 | 230 |
| K | 5��104 | 1 | 2��10-5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�
������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
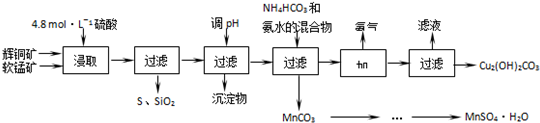
| ��ʼ������pH | ������ȫ��pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CH3OH��һ����ɫ�д̼�����ζ��Һ�壬����������������Ҫ��;��ͬʱҲ��һ����Ҫ�Ļ���ԭ�ϣ�
CH3OH��һ����ɫ�д̼�����ζ��Һ�壬����������������Ҫ��;��ͬʱҲ��һ����Ҫ�Ļ���ԭ�ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com