
分析 (1)结合N=nNA、n=$\frac{m}{M}$及分子构成计算;
(2)含有相同氧原子数的CO与CO2的物质的量比为2:1,结合V=nVm计算;
(3)Al2(SO4)3溶液中,n(Al3+):n(SO42-)=2:3,结合c=$\frac{n}{V}$计算;
(4)二价金属的氯化物中含0.2mol Cl-,则氯化物的物质的量为0.1mol,结合M=$\frac{m}{n}$计算;
(5)n(CO)=$\frac{6.72L}{22.4L/mol}$=0.3mol,发生3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,结合m=nM计算.
解答 解:(1)0.2g H2含有H原子为$\frac{0.2g}{2g/mol}$×2×NA=1.204×1023个,故答案为:1.204×1023;
(2)含有相同氧原子数的CO与CO2的物质的量比为2:1,由V=nVm可知,体积比为2:1,故答案为:2:1;
(3)Al2(SO4)3溶液中,n(Al3+):n(SO42-)=2:3,n(Al3+)=0.20mol,则其中c(SO42-)=$\frac{0.30mol}{0.1L}$=3.0mol•L-1,故答案为:3.0;
(4)二价金属的氯化物中含0.2mol Cl-,则氯化物的物质的量为0.1mol,此氯化物的摩尔质量为$\frac{9.5g}{0.1mol}$=95 g•mol-1,该金属元素的相对原子质量为95-35.5×2=24,
故答案为:95 g•mol-1;24;
(5)n(CO)=$\frac{6.72L}{22.4L/mol}$=0.3mol,发生3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,可知恰好完全反应后,剩余固体的质量为0.2mol×56g/mol=11.2g,故答案为:11.2.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、质量、体积、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 混合气体中一定有甲烷 | B. | 混合气体中一定是甲烷和乙烯 | ||
| C. | 混合气体中可能有乙烷 | D. | 混合气体中可能有乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用过量NaOH溶液除去镁粉中的铝粉 | B. | AlCl3溶液和氨水制备Al(OH)3沉淀 | ||
| C. | 用盐酸和AgNO3溶液鉴定Cl- | D. | 用加热的方法鉴别Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 ;Y元素在周期表中的位置是第三周期第VIA族.
;Y元素在周期表中的位置是第三周期第VIA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.8 g熔融KHSO4 与3.9 g熔融Na2O2 中阴离子数目相同 | |
| B. | 某金属阳离子的结构示意图为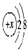 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 | |
| C. | 二硫化碳与二氧化碳结构相似,其电子式为 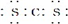 | |
| D. | 中子数为18的氯原子可表示为18Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g O2一定条件下与一定量的钠反应转移的电子数一定为2NA | |
| B. | 14 g乙烯和丙烯的混合气体中总原子数为3NA | |
| C. | 1L1 mol/L饱和FeCl3溶液滴入沸水中完全水解生成NA个氢氧化铁胶体粒子 | |
| D. | 0.1 mol•L-1 氢氧化钠溶液中所含钠离子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 金属材料都是导体,非金属材料都是绝缘体 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若Y的原子序数为m,X的原子序数一定是m±6 | |
| B. | X、Y可以属于同一周期,也可以属于不同周期 | |
| C. | X与Y一定不属于同一主族 | |
| D. | XY一定是离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com