
科目:高中化学 来源: 题型:
下列物质间的反应,属于放热反应的是( )
A.碳酸钙的分解 B.碳与氧化铜加热条件下的反应
C.Ba(OH)2·8H2O晶体和NH4Cl晶体混合 D.H2与O2在点燃条件下的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电
电压,高铁电池的总反应为
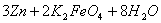

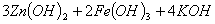
下列叙述不正确的是
A.充电时阳极反应为: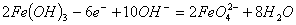
B.放电时负极反应为: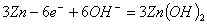
C.放电时每转移3mol电子,正极有1molK2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2是最重要温室气体,如何降低大气中CO2的含量及有效地开发利用CO2具有重大意义。
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.25 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
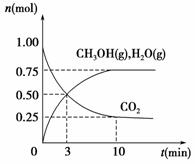
①写出该反应的化学方程式_______________________ 计算从反应开始到3 min时,氢气的平均反应速率v(H2)=____________________。
②下列措施中一定能使CO2的转化率增大的是___________________ 。
A 在原容器中再充入1 mol H2 B 在原容器中再充入1 mol CO2
C 缩小容器的容积 D 使用更有效的催化剂
E.在原容器中充入1 mol He F.将水蒸气从体系中分离出
(2)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为:2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,
CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,
(3)在一定压强下,测得该反应的实验数据如表所示。请根据表中数据回答下列问题。
|
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
①上述反应的a________0(填“大于”或“小于”)。
②恒温下,向反应体系中加入固体催化剂,则该反应的反应热a值________(填“增大”、“减小”或“不变”)。
③在一定温度下,增大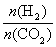 的值,CO2转化率_________,生成乙醇的物质的量________(填“增大”、“减小”、“不变”或“不能确定”)。
的值,CO2转化率_________,生成乙醇的物质的量________(填“增大”、“减小”、“不变”或“不能确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.元素性质的周期性变化是指原子半径、元素的主要化合价及原子核外电子排布的周期性变化
B.元素性质的周期性变化决定于元素原子结构的周期性变化
C.从Li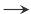 F, Na
F, Na 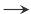 Cl,元素的最高化合价均呈现从 +1价
Cl,元素的最高化合价均呈现从 +1价  +7价的变化
+7价的变化
D.电子层数相同的原子核外电子排布,其最外层电子数均从1个到8个呈现周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种短周期元素,其元素特征信息如下表:回答下列问题:
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1) 写出下列元素的名称:C E
(2) 写出A、B、C形成的化合物M的电子式
(3) 实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为
(4) D单质与M的水溶液反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
对于在一定条件下进行的化学反应:2SO2+O2 2SO3,改变下列条件,可以提高反应物中活化分子百分数的是 ( )
2SO3,改变下列条件,可以提高反应物中活化分子百分数的是 ( )
A、增大压强 B、降低温度
C、加入催化剂 D、减小反应物浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com