
| A.镀层被划破后,镀锌的铁制品比镀锡的铁制品耐腐蚀 |
| B.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| C.铝片不用特殊方法保存 |
| D.锌跟稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快 |


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
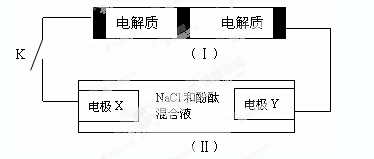
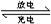 Na2S4+3NaBr。当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr。当闭合开关K时,X电极附近溶液变红。下列说法正确的是| A.闭合开关K时,钠离子从右到左通过离子交换膜 |
| B.闭合开关K时,负极反应式为:3NaBr-2e-=NaBr3+2Na+ |
| C.闭合开关K时,X电极反应式为:2Cl--2e-=Cl2↑ |
| D.闭合开关K时,当有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2H++2e-=H2↑ | B.2H2O+O2+4e-=4OH- |
| C.Fe-2e-=Fe2+ | D.4OH--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.埋在潮湿土壤里的铁管比在干燥的土壤里更容易腐蚀 |
| B.在空气里金属银的表面生成一种黑色物质 |
| C.为保护海轮的船壳,常在船壳上镶上锌块 |
| D.镀银的铁制品,镀层损坏后,露出的铁表面更容易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
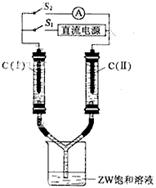
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在某些工具的机械转动部位刷油漆以防锈 |
| B.衣架和电线外面包上一层塑料层以防锈 |
| C.在钢材制造的大型船舶上装上一定数量的锌块。 |
| D.自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
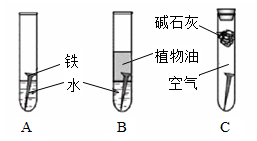
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
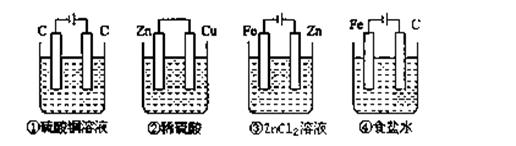
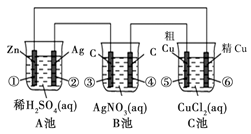
| A.④②①③ | B.④③①② | C.④③②① | D.①③②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com