
| |||||||||||||||||||||||||||||||||
(1) |
答案: MnO2+2Cl-+4H+讲析:装置 A用于制取氯气. |
(2) |
答案:除去氯气中混有的氯化氢 ,能讲析:装置 B中的饱和食盐水用于吸收氯气中混有的氯化氢,避免氯化氢与氢氧化钠溶液反应.装置C用于干燥氯气.由于是用氯气与氢氧化钠的水溶液反应制取84消毒液,故氯气可以不干燥. |
(3) |
答案:降低反应的温度,防止发生副反应生成 NaClO3讲析:根据 3X2+6OH- |
(4) |
答案:次氯酸 (或HClO) 强氧化 密封 有道理,醋酸的酸性比次氯酸的强,在消毒液中滴加醋酸有利于生成次氯酸讲析: 84消毒液中起作用的物质是次氯酸,利用了它的强氧化性,保存时要密封,避免吸收空气.醋酸、碳酸、次氯酸的酸性依次减弱,在84消毒液中滴加醋酸有利于次氯酸的生成,而醋酸本身也能消毒,一起使用效果应该更好. |
(5) |
讲析:根据氧化还原反应的原理,一部分氯元素的化合价升高,另一部分氯元素的化合价降低.在碱溶液中不存在氯气,次氯酸钠的还原产物是氯化钠,最终的氧化产物是氯酸钠. 本题以氯气的制备和氯气的性质为载体,联系社会热点新闻命题,考查同学们解决实际问题的能力. 点评:本题将氯气的制取、净化、氯气与碱溶液的反应结合起来,并联系新信息提出问题.解题的关键是理解两个新反应方程式: 3X2+6OH- |


科目:高中化学 来源:南昌二中2008届高三第一次考试化学试卷 题型:058
近年来全世界经历了多种传染性疾病(如非典、疯牛病、高致病性禽流感等)的袭扰,因此,经常性地对环境进行消毒,是预防各种传染性疾病的有效措施.某研究小组为制备消毒液(主要成分是NaClO),设计了A、B两套装置(B装置中电极材料均为石墨).并查阅到下列资料:在加热的情况下卤素单质和碱液发生如下反应:
3X2+6OH-![]() 5X-+
5X-+![]() +3H2O
+3H2O
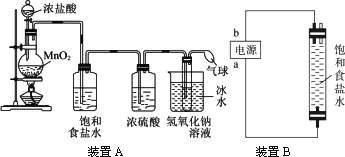
请完成下列问题:
(1)写出装置A烧瓶中发生反应的化学方程________.
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的________(填“能”或“不能”).
(3)装置A中盛冰水的烧杯的作用是________________.
(4)利用装置B制备消毒液时有关反应的化学方程式为________.
(5)装置B中a端应接电源的________极,理由是_________________________.
查看答案和解析>>
科目:高中化学 来源:贵州省白云二中2009届高考专题复习化学测试卷第四部分卤素 题型:058
近年来全世界经历了多种传染性疾病(如非典、疯牛病、高致病性禽流感等)的袭扰,因此,经常性地对环境进行消毒,是预防各种传染性疾病的有效措施.某研究小组为制备消毒液(主要成分是NaClO)设计了A、B两套装置(B装置中电极材料均为石墨).并查阅到下列资料:“在加热的情况下卤素单质和碱液发生如下反应:
3X2+6OH-![]() 5X-+XO3-+3H2O”
5X-+XO3-+3H2O”
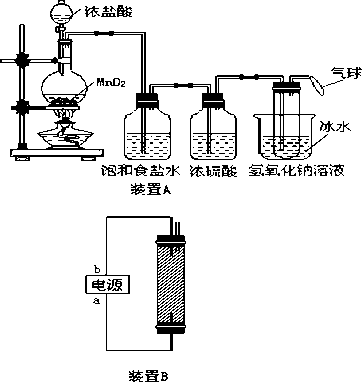
请回答下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式:
________________________________________;
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的________填“能”或“不能”)
(3)装置A中盛冰水的烧杯的作用是________;
(4)利用装置B制备消毒液时有关反应的化学方程式为:________;
(5)装置B中a端应接电源的________极,理由是________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
3X2+6OH-![]() 5X-+
5X-+![]() +3H2O
+3H2O
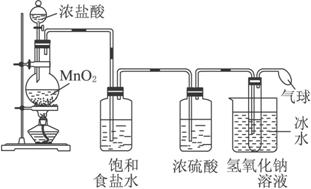
装置A
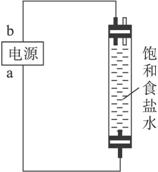
装置B
请完成下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式________________________________ 。
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的_________(填“能”或“不能”)。
(3)装置A中盛冰水的烧杯的作用是_________________________________________。
(4)利用装置B制备消毒液时有关反应的化学方程式为__________________________。
(5)装置B中a端应接电源的_________极,理由是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
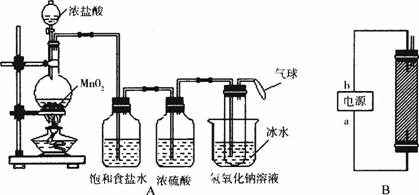
图11-7
请回答下列问题:
(1)写出装置A烧瓶中发生反应的化学方程式:_______________________________________。
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的?__________(填“能”或“不能”)。
(3)装置A中盛冰水的烧杯的作用是____________________________________________。
(4)装置B制备消毒液时有关反应的化学方程式为_________________________________。
(5)a端应接电源的__________极,理由是____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com