


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:不详 题型:填空题
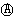 为电流表)。请回答:
为电流表)。请回答: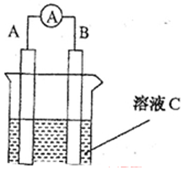
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
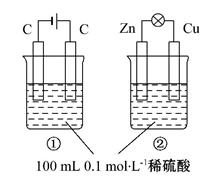
| 选择 | 叙 述 | 评价 |
| A | 装置名称:①电解池,②原电池 | 错误 |
| B | 硫酸浓度变化:①增大,②减小 | 错误 |
| C | 电极反应式:①阳极:4OH--4e-====2H2O+O2↑ ②正极:Zn-2e-====Zn2+ | 正确 |
| D | 离子移动方向:①H+向阴极移动 ②H+向正极移动 | 正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
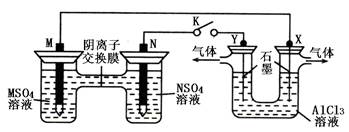
| A.溶液中c(M2+)减小 |
| B.N的电极反应式:N=N2++2e— |
| C.X电极上有H2产生,发生还原反应 |
| D.反应过程中Y电极周围生成白色胶状沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该仪器工作时酒精浓度越大,则电流强度越大 |
| B.工作时处电路电子流向为X→Y |
| C.检测结束后,X极区的pH增大 |
| D.电池总反应为2CH3CH2OH+O2=2CH3CHO+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放电时,LiMn2O4发生氧化反应 |
| B.放电时,正极反应为:Li++LiMn2O4+e-==Li2Mn2O4 |
| C.充电时,LiMn2O4发生氧化反应 |
| D.充电时,阳极反应为:Li++e-==Li |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在熔融电解质中,O2-由负极移向正极 |
| B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O |
| C.通入空气的一极是负极,电极反应为:O2 + 4e- = 2O2- |
| D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
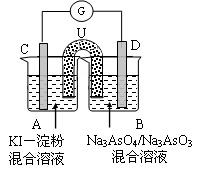

 AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为
AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2Al(s)十2NaOH(aq)+2H2O(1)=2NaAlO2(ag)+3H2(g);△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(1);△H >0 |
| C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H <0 |
D.FeCl3(aq)十3H2O(1)  Fe(OH)3(s)+3HCl(aq);△H >0 Fe(OH)3(s)+3HCl(aq);△H >0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com