




| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
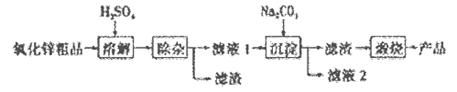
| A����Ӧ��Ϊ������ԭ��Ӧ����Ӧ��Ϊ���ֽⷴӦ |
| B����Ӧ�������������뻹ԭ�������ʵ���֮��Ϊ2��9 |
| C����Ӧ�ڵIJ���K2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ���ɱ������ |
| D������2molFeCl3������Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ6mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�������ԣ�MnO >Cl2>Fe3�� >I2 >Cl2>Fe3�� >I2 |
| B��FeCl3�������������л�ԭ�� |
| C����FeI2��Һ��ͨ��������Cl2��������Ӧ�ķ���ʽΪ6FeI2+3Cl2=2FeCl3+4FeI3 |
| D��FeCl3��ʹʪ��ĵ��۵⻯����ֽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������40��0LN2����״���� | B����0��250molKNO3������ |
| C��ת�Ƶ��ӵ����ʵ���Ϊ2��5mol | D����������Nԭ�ӵ����ʵ���Ϊ3��75mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
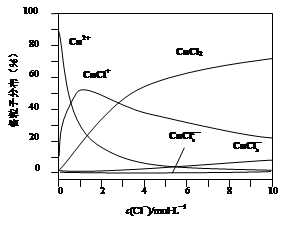
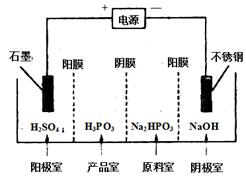
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������˪Ϊ1.98mg |
| B���ֽ����������Ϊ0.672ml |
| C������˪��Ӧ��пΪ3.90mg |
| D��ת�Ƶĵ�������Ϊ6��10�D5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0��4 mol | B��0��6 mol |
| C��0��8 mol | D��0��2 mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com