
【题目】常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是 ( )

A. 沉淀乙一定有BaCO3,可能有BaSO4
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子
D.生成的甲、乙、丙气体均为无色的易溶于水气体
【答案】C
【解析】
试题分析:由溶液pH=1可知溶液为酸性溶液,氢离子浓度为0.1mol/L,溶液中一定不存在与氢离子反应的离子:CO32-、CO32-;溶液A中加过量(NH4)2CO3,产生白色沉淀,可以排除Fe2+、Fe3+,原溶液中一定有Al3+;溶液乙加铜和浓硫酸能产生NO,原溶液中有NO3-,强酸性溶液中有NO3-,则一定没有Fe2+、I-。
A.根据分析可知,溶液中含有硫酸根离子,所以沉淀乙中一定为碳酸钡和硫酸钡沉淀的混合物,A项错误;B.根据反应方程式3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O可知,消耗14.4g铜,生成一氧化氮气体的物质的量为:14.4g÷64g/mol=0.15mol,由于没有告诉是标准状况下,0.15mol一氧化氮的体积不一定为3.36L,B项错误;C.根据以上分析可知,溶液中存在0.1mol/L的氢离子、0.1mol/L的铝离子,溶液中阳离子带有的电荷为:0.4mol/L;而溶液中除了存在0.1mol/L的硝酸根离子外,还应该含有SO42-离子和Cl-,所以该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子,C项正确;D.产生的气体NO、CO2、NH3中,NO不溶于水,D项错误;答案选C。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如右图所示。W元素的简单离子半径在同周期元素的简单离子中最小。下列说法中正确的是 ( )

A. Y元素的气态氢化物易液化,是因为其分子间能形成氢键
B. X元素最高价氧化物分子的比例模型为![]()
C. Z单质与X元素最高价氧化物、Y单质都能反应,体现氧化性
D. W的单质在地壳含量丰富,工业上可通过电解它的无水盐来制备。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列五组物质:A、O2和O3
B、![]() 和
和![]()
C、CH4与C7H16
D、CH3CH2CH2CH3与![]()
E、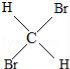 与
与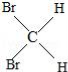
(1) 组两种物质互为同位素;
(2) 组两种物质互为同素异形体;
(3) 组两种物质互为同系物;
(4) 组两种物质互为同分异构体;
(5) 组两种物质实为同一物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 硬脂酸甘油酯和乙酸乙酯都属于酯类物质,都能发生皂化反应
B. 制造纸张的原料棉花、制造毛皮大衣的原料皮革,它们的主要成分都是纤维素
C. 在淀粉水解液中加过量NaOH,滴加碘水,如溶液未显蓝色,则证明淀粉水解完全
D. 体积分数75%的乙醇溶液可用于医疗消毒,原理是乙醇使细菌的蛋白质发生变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名化学家徐光宪获得“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法不正确的是( )
A. 铈(Ce)元素在自然界中主要以化合态形式存在
B. 铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI = CeI4 + 2H2↑
C. 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+ = Ce3++Fe3+
D. 四种稳定的核素![]() 、
、![]() 、
、![]() 、
、![]() ,它们互称为同位素
,它们互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A. 碘单质升华,克服的是其分子间作用力
B. 金刚石、石墨、纳米碳管是碳元素的同素异形体
C. 目前科学家还无法实现对原子或分子的操纵
D. HCl气体溶于水后,共价键被破坏,从而形成了H+和Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
I.污染物SO2、NOx经O2预处理后用CaSO3悬浊液吸收,可减少尾气中SO2、NOx的含量。T℃时,O2氧化烟气中SO2、NOx的主要反应的热化学方程式为:
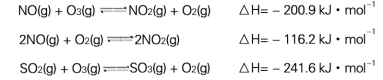
(1) T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的△H= kJ·mol-1。
3NO2(g)的△H= kJ·mol-1。
(2) T℃时,将0.6 mol NO和0.2 molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
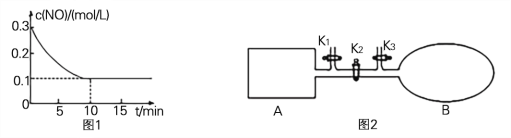
① T℃时,反应3NO(g) +O3 (g) ![]() 3NO2 (g)的平衡常数K= 。
3NO2 (g)的平衡常数K= 。
② 不能说明反应达到平衡状态的是 (填写字母)。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1∶3
II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题:
(3) 如图2所示,A是由导热材料制成的恒容密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
① 容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)= 。
② 平衡后在A容器中再充入0.5 mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数(填“变大”、“变小”或“不变”) 。
③ 在②平衡后,打开K2,重新到达新平衡,B气囊的体积为0.8aL,则在打开K2之前,气囊B的体积为 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com