
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |
| B. | 乙醇与钠反应:2CH3CH2O-+2H++2Na→2CH3CH2ONa+H2↑ | |
| C. | 苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 苯酚溶液中加入溴水: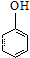 +3B2→ +3B2→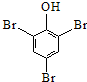 ↓+3H++3Br- ↓+3H++3Br- |
分析 A.乙酸为弱酸,离子方程式中乙酸需要保留分子式;
B.乙醇钠为强电解质,离子方程式中需要拆开;
C.苯酚的酸性大于碳酸氢根离子,二者反应生成苯酚和碳酸氢根离子;
D.苯酚与浓溴水反应生成三溴苯酚和溴化氢.
解答 解:A.CH3COOH为弱酸,在离子方程式中应写成化学式,正确的反应的离子方程式为:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故A错误;
B.乙醇与钠反应生成乙醇钠和氢气,乙醇钠应该拆开,正确的离子方程式为:2CH3CH2O-+2H++2Na→2CH3CH2O-+2Na++H2↑,故B错误;
C.苯酚钠溶液中通入二氧化碳,反应生成苯酚和碳酸氢钠,正确的离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D.苯酚溶液中加入溴水,反应生成三溴苯酚,反应的离子方程式为: +3B2→
+3B2→ ↓+3H++3Br-,故D正确;
↓+3H++3Br-,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;C为易错点,注意苯酚的酸性大于碳酸氢根离子,二者反应生成苯酚和碳酸氢根离子.


科目:高中化学 来源: 题型:选择题
| A. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| B. | 用牺牲锌块的方法来保护船身 | |
| C. | 用铜质铆钉铆接铁板,铁板不易被腐蚀 | |
| D. | 浸泡在水中钢闸门,水面附近区域的腐蚀程度大于长期在水下的部分 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
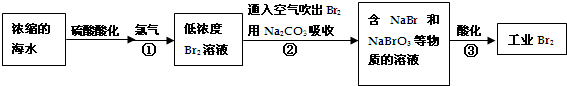
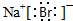 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 完全燃烧产物只有二氧化碳和水 | |
| B. | 它们几乎不溶于水 | |
| C. | 分子的通式为CnH2n+2,与氯气发生取代反应 | |
| D. | 它们完全由碳氢元素组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
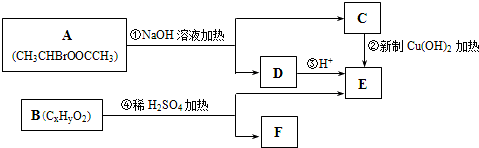
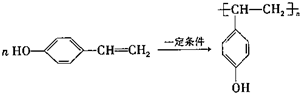 .
.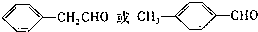 等.
等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
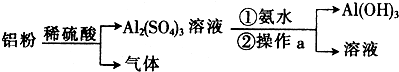
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,可以加快反应速率 | |
| B. | 降低温度,可以加快反应速率 | |
| C. | 在上述条件下,SO2能完全转化为SO3 | |
| D. | 任何情况,达到平衡时,SO2和SO3的浓度都一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、蛋白质均属于高分子化合物,油脂不属于高分子化合物 | |
| B. | 乙醇的分子式为C2H6O,常温下是一种无色液体,密度比水小 | |
| C. | 乙酸的结构简式是CH3COOH,能和水以任意比互溶,酸性比碳酸强 | |
| D. | 乙烯是重要的化工原料,能使溴水和酸性高锰酸钾溶液褪色,具有漂白作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com