
【题目】分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15:2:8,其中化合物A的质谱图如图.
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1:1:2,它能够发生银镜反应.B为五元环酯.C的红外光谱表明其分子中存在甲基.其它物质的转化关系如下:
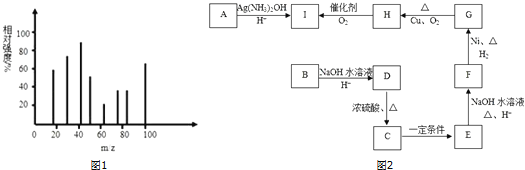
(1)A的分子式是: .
(2)B和G的结构简式分别是: 、 .
(3)写出下列反应方程式(有机物用结构简式表示)
D→C ;
H→G .
(4)写出由单体F发生缩聚反应生成的产物的结构简式: .
【答案】(1)C5H8O2;(2)![]() 、 CH2(OH)CH2CH2CH2COOH;
、 CH2(OH)CH2CH2CH2COOH;
(3)CH3CH(OH)CH2CH2COOH![]() CH3CH=CHCH2COOH+H2O;OHCCH2CH2CH2COOH+H2
CH3CH=CHCH2COOH+H2O;OHCCH2CH2CH2COOH+H2![]() CH2(OH)CH2CH2CH2COOH;(4)
CH2(OH)CH2CH2CH2COOH;(4)![]() 。
。
【解析】
试题分析:A、B、C互为同分异构体,根据它们分子中C、H、O元素的质量比为15:2:8,可以确定其分子中原子个数比为![]() :
:![]() :
:![]() =5:8:2,所以A的最简式为C5H8O2,根据A的质谱图知确定A的相对分子质量是100,所以A的分子式为C5H8O2,A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1:1:2,它能够发生银镜反应,则A中含有醛基,A的不饱和度=
=5:8:2,所以A的最简式为C5H8O2,根据A的质谱图知确定A的相对分子质量是100,所以A的分子式为C5H8O2,A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1:1:2,它能够发生银镜反应,则A中含有醛基,A的不饱和度=![]() =2,A的结构简式为OHCCH2CH2CH2CHO;B为五元环酯,则B的结构简式为
=2,A的结构简式为OHCCH2CH2CH2CHO;B为五元环酯,则B的结构简式为![]() ,C的红外光谱表明其分子中存在甲基,B水解然后酸化得D,D的结构简式为CH3CH(OH)CH2CH2COOH,A发生银镜反应生成I,I的结构简式为HOOCCH2CH2CH2COOH;D发生消去反应生成C,C发生取代反应生成E,E和氢氧化钠的水溶液发生取代反应生成F,F和氢气发生加成反应生成G,G发生氧化反应生成H,H发生氧化反应生成I,根据I的结构简式结合题给信息知,C的结构简式为CH3CH=CHCH2COOH,E为CH2ClCH=CHCH2COOH,F为CH2(OH)CH=CHCH2COOH,G为CH2(OH)CH2CH2CH2COOH,H为OHCCH2CH2CH2COOH,(1)通过以上分析知,A的分子式为C5H8O2;(2)通过以上分析知,B的结构简式为
,C的红外光谱表明其分子中存在甲基,B水解然后酸化得D,D的结构简式为CH3CH(OH)CH2CH2COOH,A发生银镜反应生成I,I的结构简式为HOOCCH2CH2CH2COOH;D发生消去反应生成C,C发生取代反应生成E,E和氢氧化钠的水溶液发生取代反应生成F,F和氢气发生加成反应生成G,G发生氧化反应生成H,H发生氧化反应生成I,根据I的结构简式结合题给信息知,C的结构简式为CH3CH=CHCH2COOH,E为CH2ClCH=CHCH2COOH,F为CH2(OH)CH=CHCH2COOH,G为CH2(OH)CH2CH2CH2COOH,H为OHCCH2CH2CH2COOH,(1)通过以上分析知,A的分子式为C5H8O2;(2)通过以上分析知,B的结构简式为![]() ,G为CH2(OH)CH2CH2CH2COOH;(3)D的结构简式为CH3CH(OH)CH2CH2COOH,C的结构简式为CH3CH=CHCH2COOH,D发生消去反应生成C,反应方程式为:CH3CH(OH)CH2CH2COOH
,G为CH2(OH)CH2CH2CH2COOH;(3)D的结构简式为CH3CH(OH)CH2CH2COOH,C的结构简式为CH3CH=CHCH2COOH,D发生消去反应生成C,反应方程式为:CH3CH(OH)CH2CH2COOH![]() CH3CH=CHCH2COOH+H2O,G为CH2(OH)CH2CH2CH2COOH,H为OHCCH2CH2CH2COOH,G发生氧化反应生成H,反应方程式为OHCCH2CH2CH2COOH+H2
CH3CH=CHCH2COOH+H2O,G为CH2(OH)CH2CH2CH2COOH,H为OHCCH2CH2CH2COOH,G发生氧化反应生成H,反应方程式为OHCCH2CH2CH2COOH+H2![]() CH2(OH)CH2CH2CH2COOH;(4)CH2(OH)CH=CHCH2COOH分子间羟基与羧基之间脱去水发生缩聚反应产物的结构简式为:
CH2(OH)CH2CH2CH2COOH;(4)CH2(OH)CH=CHCH2COOH分子间羟基与羧基之间脱去水发生缩聚反应产物的结构简式为:![]() 。
。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAs g·mol-1,原子半径分别为rGapm和rAspm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:

⑴ KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列 物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
⑵ 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式: 。
⑶ 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式: 。
⑷ 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是 。
⑸ 上述流程中可以循环使用的物质有石灰、CO2、 和 (写化学式)。
⑹ 若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得 mol KMnO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是 ( )
A. Cu(OH)2难溶于水,属于非电解质
B. SO2能与碱反应生成盐和水,属于酸性氧化物
C. NH4Cl组成中不含金属离子,不属于盐
D. HCl气体溶于水电离出H+和Cl-,属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0g投入盛有50mL0.1molL-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是
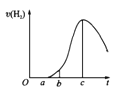
A.O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸
B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时刻,反应处于平衡
D.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】内锌矿的主要成分为ZnS,含有杂质PbS、CuS、FeS、SiO2等,以闪锌矿制备氯化锌的流程如图所示。

请回答下列问题:
(1)配制氯化铁浸渍液时要求pH为0.8~1之间,pH太高则 ,pH太低,浸渍矿石会产生有害气体 ,操作①是 。由氯化锌溶液制备氯化锌晶体的方法是 。
(2)高沸点溶剂R—4E几乎不溶于水,120℃时硫在R—4E里的溶解度为365g,室温时溶解度为35.9g,从浸出液B提取硫的方法是 。硫是工业制备硫酸的原料,现有1吨矿石,硫的总含量为24%,最多制备浓度98%的硫酸 吨。
(3)氯化铁与硫化锌发生反应:![]() ,则氯化铁与FeS反应的方程式为 。
,则氯化铁与FeS反应的方程式为 。
(4)溶液X的成分的化学式为 ,该流程中循环使用的物质是 。
(5)由氯化亚铁溶液制备氯化铁溶液,可以用![]() 、
、![]() ,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往200mL FeC13溶液中,通入0.672L标准状况下的H2S气体,气体完全被吸收,再加入过量的铁粉产生氢气,反应停止后,测得溶液中含有0.15 mol金属阳离子,求:
(1) FeC13溶液与H2S反应的离子方程式为__________________;
(2)加入过量铁粉充分反应后产生氢气在标准状况下的体积?
(3)原FeC13溶液的浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ/mol
2C(s)+O2(g)=2CO(g) ΔH=-220kJ/mol,H-H、O=O和O-H键的键能分别为436、496和462kJmol-1,则a为( )
A.-332 B.-118 C.+350 D.+130
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com