

| A.氯化铝、氯化铁、氢氧化钠 | B.氯化铝、氯化镁、氢氧化钠 |
| C.偏铝酸钠、氢氧化钡、硫酸 | D.偏铝酸钠、氯化钡、硫酸 |


科目:高中化学 来源:不详 题型:单选题
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=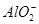 +4 +4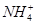 |
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液: |
C.磷酸一氢钠溶液水解: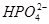 +H2O +H2O 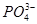 +H3O+ +H3O+ |
| D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O2溶于水产生O2:2O22—+2H2O=O2↑+4OH- |
| B.向氨水通入足量SO2:SO2+2NH3·H2O=2NH4++SO32-+H2O |
| C.次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl—+H2O=Cl2↑+2OH— |
| D.NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.溴乙烷在氢氧化钠水溶液中的反应:CH3CH2Br + OH-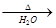 CH3CH2OH +Br- CH3CH2OH +Br- |
B.醋酸溶液与氢氧化铜反应:2CH3COOH + Cu(OH)2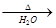 Cu2+ + 2CH3COO-+ 2H2O Cu2+ + 2CH3COO-+ 2H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+ CO2 + H2O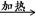 2C6H5OH + CO32- 2C6H5OH + CO32- |
D.甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH-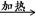 CO32-+2NH4+ +4Ag↓+6NH3+2H2O CO32-+2NH4+ +4Ag↓+6NH3+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
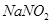 是一种食品添加剂,它与酸性
是一种食品添加剂,它与酸性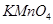 溶液的反应方程式为:
溶液的反应方程式为: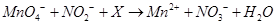 ,下列叙述中正确的是
,下列叙述中正确的是A.生成l mo1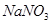 需消耗0.4mo1 需消耗0.4mo1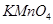 |
| B.反应过程中溶液的pH减小 |
C.该反应中NO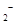 被还原 被还原 |
D.X表示的粒子是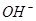 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.硫酸型酸雨的形成会涉及反应:2H2SO3+O2 2H2SO4 2H2SO4 |
B.热的纯碱溶液可以清洗油污的原因: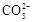 +2H2O +2H2O H2CO3+2OH¯ H2CO3+2OH¯ |
C.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH¯=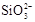 +H2O +H2O |
| D.成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl¯+ ClO¯+2H+= Cl2↑+ H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
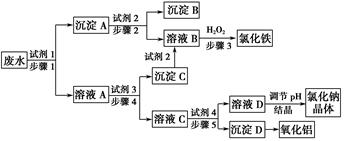
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH=Mg2++2CH3COO-+2H2O |
| B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO4-+3H2O2+6H+=2Mn2++6H2O+4O2↑ |
| C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com