
分析 (1)反应物中的原子全部参加反应的,原子利用律最高,据此解答即可;水电离的OH-的物质的量浓度=$\frac{1{0}^{-14}}{1{0}^{-PH}}$;常温下,0.1mol•L-1 KHCO3溶液pH>8,说明碳酸氢根在水解程度大于电离程度;
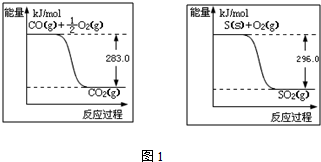
(2)由图1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
利用盖斯定律(i)-(ii)计算即可;
(3)①根据时段Ⅰ达到平衡时生成氨气的物质的量及热化学方程式N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1计算出放出的热量;
②根据25min时氨气的物质的量变为0,而氮气和氢气的物质的量不变进行解答,改变的条件是分离出氨气;
③根据时段Ⅲ条件下达到平衡时各组分的浓度及平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积进行解答;
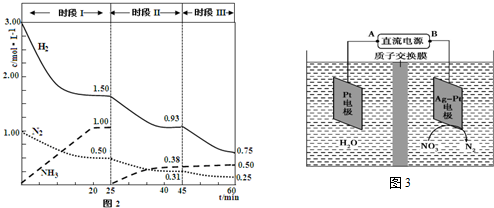
(4)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有氢离子参与反应且有水生成.
解答 解:(1)观察四个反应方程式可见,只有反应d中参加反应的物质全部转化为一种物质,故原子利用率最高;
可用碳酸钾溶液吸收生成的CO2,常温下pH=10的碳酸钾溶液中水电离的c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-PH}}$mol/L=1×10-4 mol•L-1;
常温下,0.1mol•L-1 KHCO3溶液pH>8,则溶液中碳酸氢根离子水解程度大于电离程度,所以c(H2CO3)>c(CO32-);
故答案为:d; 1×10-4 mol•L-1;>;
(2)由图1可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-563-(-298)=-270kJ•mol-1,
故答案为:-270kJ/mol;
(3)①时段Ⅰ达到平衡时生成的氨气的物质的量为:1.00 mol/L×2L=2.00mol,
根据N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1可知生成2.00mol氨气放出的热量为94.4kJ,
故答案为:94.4kJ;
②25min时氨气的物质的量迅速变为0而氮气、氢气的物质的量不变,之后氮气、氢气的物质的量逐渐减小,氨气的物质的量逐渐增大,说明25min时改变的条件是将NH3从反应体系中分离出去,
故答案为:将NH3从反应体系中分离出去;
③时段Ⅲ条件下,反应为:N2(g)+3H2(g)?2NH3(g),图象方向可知平衡状态下[N2]=0.25mol/L,[NH3]=0.50mol/L,[H2]=0.75mol/L,该反应的化学平衡常数为:K=$\frac{{c}^{2}(N{H}_{3})}{{c({N}_{2})c}^{3}({H}_{2})}$=$\frac{(0.50mol/L)^{2}}{(0.75mol/L)^{3}×0.25mol/L}$=2.37,
故答案为:2.37;
(4)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,
所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2↑+6H2O,
故答案为:A,2NO3-+12H++10e-=N2↑+6H2O.
点评 本题主要考查的是绿色化学的概念、盖斯定律的应用、影响化学平衡的因素及电解池工作原理,题目难度中等,明确化学平衡常数的概念及计算方法是解题关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 无机化合物可根据其组成和性质进行分类
无机化合物可根据其组成和性质进行分类| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素为Mn元素 | B. | 该元素最高化合价为+7 | ||
| C. | 该元素属于d区元素 | D. | 该元素原子最外层共有7个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
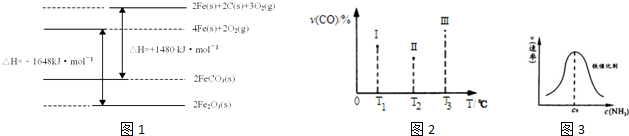
 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图表示:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 2min | 4min | 6nin | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.20 | … |
| CH2OH | 0.03 | 0.04 | 0.04 | 0.05 | … |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com