
(7分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析: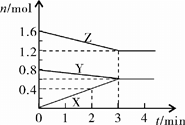
(1)该反应的化学方程式为: ;
(2)反应开始至2min末,X的反应速率为 (mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是: 。
科目:高中化学 来源: 题型:
(7分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式为: ;
(2)反应开始至2min末,X的反应速率为 (mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是: 。
查看答案和解析>>
科目:高中化学 来源:2010年河南省焦作市高一下学期期末测试化学(必修2)试题 题型:填空题
(7分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
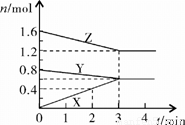
(1)该反应的化学方程式为: ;
(2)反应开始至2min末,X的反应速率为 (mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分) (1)某温度下纯水中![]() ,则此时溶液中的C(
,则此时溶液中的C(![]() )= 。若温度不变,滴入稀盐酸使
)= 。若温度不变,滴入稀盐酸使![]() ,则此时溶液中的C(
,则此时溶液中的C(![]() ) mol/L,由水电离产生的C
) mol/L,由水电离产生的C![]() = mol/L。
= mol/L。
(2)5℃时。0.1 mol/L的HCl和0.1 nml/L NH3?H2O的混合后,在下列3种情况下:①混合液pH=7;②混合液pH>7;③混合液pH<7,则这三种溶液中![]() 大小为 。(填序号)
大小为 。(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(12分)在一定条件下,可逆反应A + B![]() mC变化如右图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,P为反应在T2温度时达到平衡后向容器加压的变化情况,问:
mC变化如右图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,P为反应在T2温度时达到平衡后向容器加压的变化情况,问:
⑴温度T1 T2(填大于、等于或小于)
⑵正反应是 反应(填“吸热”或“放热”)
⑶如果A、B、C均为气体,则m 2(填大于、等于或小于)
⑷当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,
则体系的压强 (填增大、减小或不变),平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”)
22.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填“吸热”、“放热”)。
(3)能判断该反应已经达到化学平衡状态的依据是 (多选扣分)。
A、容器中压强不变;B、混合气体中c(CO)不变;C、v正(H2)=v逆(H2O);D、c(CO2)=c(CO)。
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃
23. (12分)在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2![]() 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
⑴NO2的转化率为?
⑵反应前后的压强比为多少?
⑶在这5分钟内,用O2来表示的平均反应速率是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com