
【题目】下列实验操作正确的是
A. 用激光笔验证淀粉溶液的丁达尔效应
B. 用稀硫酸洗涤并灼烧铂丝后,再进行焰色反应
C. 蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却
D. 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
科目:高中化学 来源: 题型:
【题目】肼(N2H4)可作为火箭发动机的燃料。
(1)肼(N2H4)与氧化剂N2O4(l)反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)===N2O4(l) ΔH1=195 kJ·mol1
②N2H4(l)+O2(g)===N2(g)+2H2O(g) ΔH2=534 kJ·mol1
试计算1 mol肼(l)与N2O4(l)完全反应生成N2和水蒸气时放出的热量为________,写出肼(l)和N2O4(l)反应的热化学方程式:________________________________。
(2)有关肼化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):
N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量是________ kJ。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是

A. 0-t1时,原电池的负极是铜片
B. 0-t1时,正极的电极反应式是2H++2e-=H2↑
C. t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应
D. tl时刻后,电子从铝经过导线流向铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法错误的是
A. 碘酒在处理伤口时,应用了I2的氧化性
B. 明矾净水,利用了Al(OH)3胶粒的吸附性质
C. 铁粉可以用于食品保鲜,涉及到Fe的还原性
D. 苏打水是Na2CO3饱和溶液,可以缓解胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如下图所示,且每一段只对应一个反应。下列说法正确的

A. 开始时产生的气体为H2
B. AB段产生的反应为置换反应
C. 所用混合溶液中c(HNO3)=0.5mol·L-1
D. 参加反应铁粉的总质量m2=5.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为_________(填标号)。C、D中有气泡冒出,并可观察到的现象分别为_______________。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1 molCu(OH)2后恰好恢复到电解前状态。则电解过程中转移的电子的物质的量为
A. 0.1 mol B. 0.2 mol C. 0.3 mol D. 0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关防止或减少酸雨的措施中不可行的是( )
A. 对燃煤及燃煤烟气进行脱硫
B. 推广天然气、甲醇等作为汽车的燃料
C. 对含SO2、NO2的废气处理后再排空
D. 人工收集大气雷电产生的氮的氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100 0 mol/L NaOH溶液分别滴定20.00 mL 0.100 0 mol/L盐酸和20.00 mL 0.100 0 mol/L醋酸溶液,得到2条滴定曲线,如图所示。
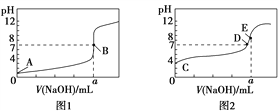
若以HA表示酸,下列说法不正确的是
A. 滴定盐酸的曲线是图1
B. 达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
C. 达到B、E状态时,反应消耗的n(CH3COOH)=n(HCl)
D. 当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com