
氮的多样性主要体现在含氮化合物及其性质的多样性上,下列说法正确的是( )
A.Fe2+、Mg2+、Cl-、NO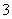 能大量共存于pH=0的溶液中
能大量共存于pH=0的溶液中
B.1 L浓度为1 mol·L-1的NH4Cl溶液中含有NA个NH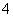
C.除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO
D.不论是浓硝酸还是稀硝酸,与铜反应均体现出硝酸的酸性和强氧化性
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
香茅醛是一种食用香精,异蒲勒醇是一种增香剂,一定条件下,香茅醛可转化为异蒲勒醇。下列说法不正确的是

A.香茅醛与异蒲勒醇互为同分异构体
B.香茅醛的分子式为C10H19O
C.异蒲勒醇可发生加成、取代、消去反应
D.鉴别香茅醛与异蒲勒醇可用Br2水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施不合理的是( )
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
向25 mL 18.4 mol/L H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量( )21教育名师原创作品
A.小于0.23 mol
B.等于0.23 mol
C.0.23 mol~0.46 mol之间
D.等于0.46 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
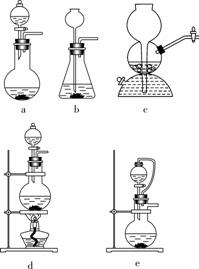
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,图中可选用的发生装置是 ae (填写字母)。
(2)若用硫酸和亚硫酸钠反应制取3.36 L(标准状况)二氧化硫,至少需要称取亚硫酸钠 18.9 g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠 19.8 g (保留一位小数)。
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为SO2+Ca(OH)2===CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O===2CaSO4·2H2O。其流程如下图:
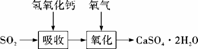
碱法的吸收反应为SO2+2NaOH===Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
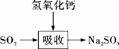
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.90 |
吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 利用SO2是酸性氧化物,可与碱反应 。和碱法相比,石灰-石膏法的优点是 原料易得,吸收成本低 ,缺点是 吸收速率慢,效率低 。21·世纪*教育网
(4)在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 L H2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状况下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是________________________________________________________________________,
乙的电子式是________________________________________________________________________。
(2)甲与水反应的化学方程式是________________________________________________________________________
________________________________________________________________________。
(3)气体丙与金属镁反应的产物是 Mg3N2 (用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式________________________________________________________________________
________________________________________________________________________。
有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之 取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,证明产物Cu中含有Cu2O;若溶液不变蓝色,证明产物Cu中不含Cu2O (已知Cu2O+2H+===Cu+Cu2++H2O)。
(5)甲与乙之间 可能 (填“可能”或“不可能”)发生反应产生H2,判断理由是 AlH3中氢元素的化合价为-1价,NH3中含有+1价的氢元素,二者可发生氧化还原反应产生H2 。
查看答案和解析>>
科目:高中化学 来源: 题型:
件下,将相同物质的量的Na、Mg、Al分别加入盛有同浓度、同体积稀盐酸的甲、乙、丙三个烧杯中充分反应,生成气体的体积关系不可能是( )
A.甲(Na)>乙(Mg)>丙(Al)
B.甲(Na)>乙(Mg)=丙(Al)
C.甲(Na)<乙(Mg)<丙(Al)
D.甲(Na)=乙(Mg)=丙(Al)
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.12 g铁粉加入25 mL 2 mol/L氯化铁溶液中充分反应后,结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B.往溶液中滴入无色KSCN溶液,溶液变红色
C.Fe2+和Fe3+物质的量之比为5∶1
D.氧化产物和还原产物的物质的量之比为2∶ 5
查看答案和解析>>
科目:高中化学 来源: 题型:
下列鉴别方法可行的是( )
A.用氨水鉴别Al3+、Mg2+和Ag+
B.用Ba(NO3)2溶液鉴别Cl-、SO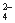 和CO
和CO
C.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷
D.用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com