
(16分)填空
(1)在1~18号元素中,除稀有气体元素外:
原子半径最大的元素是 , 电负性最大的元素_______________(用元素符号表示)
(2) 某元素 +3价离子的3d轨道半充满,该元素为_______(用元素符号表示)
(3)某元素的原子的价电子构型为4S24P1,它在周期表中的位置是 _______;最高正化合价_______;
(4)下表是短周期元素一些气态原子失去核外不同电子所需的能量,(即电离能,单位为kJ?mol-1):
电离能 | 锂 | X | Y |
I1 | 519 | 502 | 580 |
I2 | 7296 | 4570 | 1820 |
I3 | 11799 | 6920 | 2750 |
I4 |
| 9550 | 11600 |
表中X元素为 (填元素符号)。Y是周期表中 族元素。
(5)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,该元素基态原子的电子排布为 。
科目:高中化学 来源: 题型:
(16 分)某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。
【查阅资料】:草酸铵![]() 属于弱电解质:草酸钙
属于弱电解质:草酸钙![]() 难溶于水;
难溶于水;![]() 、
、![]() 、
、![]() 完全沉淀的pH;
完全沉淀的pH;![]() :
:![]() ;
;![]() ;
;![]() 。
。
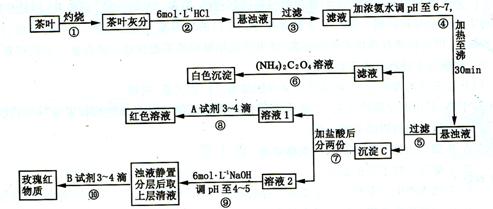
试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是__________________________。
(2)写出检验![]() 的离子方程式______________________________。
的离子方程式______________________________。
(3)写出沉淀C所含主要物质的化学式________________________。
(4)写出步骤⑧用A试剂生成血红色溶液的离子方程式____________________。
(5)步骤⑨的作用是__________,发生反应的离子方程式____________________。
(6)猜测步骤⑩的目的是____________________________。
(7)已知:![]() ,
,![]() ;
;![]() ;
;![]() ,则
,则![]() _______
_______![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省南安一中高一下学期期中考试化学试卷(带解析) 题型:填空题
(本小题满分16分)
Ⅰ.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染源的方法可以有 (多选扣分)
a.开发氢能源 b.使用电动车 c.植树造林 d.戴上呼吸面具
Ⅱ.A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图, B的最外层电子数比K层电子多1,
B的最外层电子数比K层电子多1,
D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
(1) 指出元素A在周期表中的位置 ,其气态氢化物的化学式为 。
(2) D和E两种元素相比较,非金属性较强的是(填元素符号) ,
可以验证该结论的是(填写字母序号) ;
A.比较这两种元素的常见单质的熔沸点 B.比较这两种元素的气态氢化物的熔沸点
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素置换能力的强弱
(3)C、D、E三种元素最高价氧化物的水化物的酸性由强到弱的顺序: 。(填写化学式)
查看答案和解析>>
科目:高中化学 来源:2015届陕西省高一第三次月考化学试卷(解析版) 题型:填空题
(16分) 某校化学兴趣小组的同学经查阅资料得知:铝表面致密的氧化膜能使铝与其周围的介质(空气、水等)隔绝,但奇怪的是铝制容器仍不能用来盛放和腌制咸菜。为此该小组的同学对铝表面的氧化膜进行了探究,其过程如下,请完成下列填空。
(1)用坩埚钳夹住一块擦去氧化膜的铝片,放在酒精灯火焰上灼烧,铝片表面接触火焰的部分变暗,片刻后变软,轻轻摇动,会左右摇晃,却不像蜡烛那样滴落。这是因为铝表面氧化膜的熔点________(填“高于”或“低于”)内层铝的熔点,并将其裹住,所以不易发生滴落现象。
(2)取纯净的铝箔,包裹住一小块金属钠后放入水中无现象;将该铝箔用针刺些小孔后再包裹住一小块金属钠后放入水中,迅速就有大量的气泡产生。试解释其中的原因,并写出相关的化学方程式:___________ ___________________。
(3)用砂纸打磨一铝片,使其表面变粗糙,再将其放入CuSO4稀溶液中,2~3 min后有少量红色固体附着在其表面。试写出产生红色固体的离子方程式: 。
(4)把两块未用砂纸打磨过的铝片都浸入氢氧化钠溶液中,片刻后其表面产生无色气体。试写出铝的氧化膜与氢氧化钠溶液反应的离子方程式:___________________________。
(5)另取一铝制易拉罐,收集满一罐CO2,加入过量的浓氢氧化钠溶液,立即把口封闭。可以发现易拉罐“咔咔”作响,并变瘪了;过一会后,易拉罐又会作响并鼓起来。试解释为什么,写出有关的离子方程式
查看答案和解析>>
科目:高中化学 来源:2014届江苏省高一第一学期期中考试化学试卷 题型:填空题
(本小题满分16分)
Ⅰ.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染源的方法可以有 (多选扣分)
a. 开发氢能源 b. 使用电动车 c. 植树造林 d.戴上呼吸面具
Ⅱ.A、B、C、D、E五种短周期元素,原子序数E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子结构示意图如图, B的最外层电子数比K层电子多1,
B的最外层电子数比K层电子多1,
D元素的主族序数是周期序数的2倍,E的单质是黄绿色气体;据此填空:
(1) 指出元素A在周期表中的位置 ,其气态氢化物的化学式为 。
(2) D和E两种元素相比较,非金属性较强的是(填元素符号) ,
可以验证该结论的是(填写字母序号) ;
A.比较这两种元素的常见单质的熔沸点 B.比较这两种元素的气态氢化物的熔沸点
C.比较这两种元素的气态氢化物的稳定性 D.比较这两种元素置换能力的强弱
(3)C、D、E三种元素最高价氧化物的水化物的酸性由强到弱的顺序: 。(填写化学式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com