
����һ����NaOH��Һ�У���ͨ��һ���� CO2����ַ�Ӧ����Һ��һ�������½������ɣ��õ��������ʡ�������m ��ͨ���������V(CO2)�Ĺ�ϵ��ͼ������˵����ȷ����

A���������ʣ�a����NaOH��b����Na2CO3 ��c����NaHCO3
B��a��b �� b��c ���ι��̵õ��ľ��壬������ͬ�ľ�������
C�����������е���Һ��һ�����ں��ʽ��c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-)
D����ͨ��V2=1��344 L (���) ���壬��m2=13��12 g
BD
��������
���������
A��b����Na2CO3��10H2O������B������Na2CO3���壬��ȷ��C������غ㣺c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-)������
D����ȷ�� nNaOH =4/40=0��1 nCo2= 1��344/22��4=0��06
2 Na OH+ CO2 = Na2CO3+ H2O Na2CO3+ H2O+ CO2 = 2 NaHCO3
2 1 1 1 1 2
0��1 0��05 0��05 0��01 0��01 0��02
Na2CO3��10H2O: 0��05 - 0��01=0��04 NaHCO3: 0��02
m��=m NaHCO3 +m Na2CO3��10H2O =0��02*84+0��04*286=13��12��g��
���㣺���黯ѧͼ������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
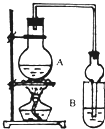 I������ʵ����ơ�������ʵ�������������
I������ʵ����ơ�������ʵ�������������| �Լ� | ���� | �Ҵ� | ���� | �������� |
| �е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�꽭��ʡ�ձ����и�������ĩͳ����ѧ�Ծ��������棩 ���ͣ������
�ߴ���ϸ�������������ںϳ�����﮵�ص缫���ϣ���ҵ�Ͽ�������ȡ�Ѱ۵ĸ���Ʒ�̷���FeSO4��7H2O��ͨ�����з�Ӧ�Ʊ���
FeSO4��2NH3��H2O��Fe(OH)2����(NH4)2SO4
Fe(OH)2��H2C2O4��FeC2O4��2H2O
��1���̷��к���һ������TiOSO4���ʡ����̷�����ϡ���ᣬ�������ۡ����衢��ַ�Ӧ������һ��ʱ�䣬���ˣ��ɵô�����FeSO4��Һ�������������У�TiOSO4����ˮ��Ӧת��ΪH2TiO3������д���÷�Ӧ�Ļ�ѧ����ʽ�� ���������۵������� �� ��
��2���ɴ�����FeSO4��Һ��ȡFeC2O4ʱ��������ջ����½��У�ԭ���� ��
FeC2O4���ɺ�Ϊ��߲�Ʒ���ȣ����������ҺpH��2����pH���ͣ�����
FeC2O4�IJ��� ���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
��3��������FeC2O4�Ļ��Һ���ˣ�����Ʒ����ˮϴ�ӣ�������ˮ�Ҵ���ϴ����ˮ�Ҵ��������� �� ��
��4��ij�о�С������ij������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3�����������Ʊ��ϴ�����FeSO4��Һ���ٺϳ�FeC2O4���벹�������ɸû��������Ʊ��ϴ�����FeSO4��Һ��ʵ�鲽�裨��ѡ�õ��Լ������ۡ�ϡ�����NaOH��Һ������һ�����û��������м���������ϡ�����ַ�Ӧ�����ˣ� �����ˣ��õ��ϴ�����FeSO4��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡģ���� ���ͣ������
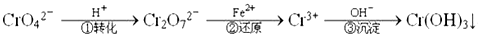
 Cr2O72��(��ɫ)+H2O
Cr2O72��(��ɫ)+H2O  Cr3+(aq)+3OH-(aq) �����£�Cr(OH)3���ܶȻ�Ksp=10-32��Ҫʹc(Cr3+)����10-5mol/L����Һ��pHӦ����_____��
Cr3+(aq)+3OH-(aq) �����£�Cr(OH)3���ܶȻ�Ksp=10-32��Ҫʹc(Cr3+)����10-5mol/L����Һ��pHӦ����_____�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
I����ʵ����ơ�������ʵ�������������_________������ţ�
A������ά�غ������Ϲ��Ⱥ��Һ�壬ȡ���������������Ƶ�Cu(OH)2����Һ���ȣ��۲��Ƿ���ש��ɫ�������ɣ���֤����ά��ˮ������������
B��Һ̬�������м���ϡNaOH��Һ�����ӣ�Ȼ���������ϡHNO3���ټ���AgNO3��Һ����Br��������
C������������Ƿ���м�ȩ��������Ʒ�м�������NaOH��Һ���к�HCOOH������������Ӧʵ��
D�����뱽�ͱ��ӵĻ��Һ����������Ũ��ˮ�����ˣ����ɷ���
E����ͭ˿�ھƾ��������ϼ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ
F����ȡ�ܽ���ˮ�е������⣺����ƾ��������÷ֲ��ȡ���л����ٷ���
G�����Թ��м���2mL10%��CuSO4��Һ������2%��NaOH��Һ4��6�Σ��������ȩ��Һ0.5mL�����������ڣ�֤����ȩ������
 II ��֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2��6C2H5OH��
II ��֪������ˮ�Ȼ��ƿ����Ҵ��γ�������ˮ��CaCl2��6C2H5OH��
���й��л���ķе㣺
| �Լ� | ���� | �Ҵ� | ���� | �������� |
| �е㣨�棩 | 34.7 | 78.5 | 118 | 77.1 |
ij����С����Ƶ�ʵ������ȡ�϶�������������װ����ͼ��ʾ��A�з��й����Ҵ�����ˮ�����ƺ�Ũ���ᣬB�з��б���̼������Һ���Իش�
��1��A��Ũ�����������
��Ӧ�м�����Ҵ��ǹ����ģ���Ŀ����________________________________��
��2������ͬλ��18Oʾ�ٷ�ȷ����Ӧ����ˮ��������ԭ�ӵ��ṩ�ߣ�д���ܱ�ʾ18Oλ�õĻ�ѧ��Ӧ����ʽ ��
��3����ʵ����ʹ�����ιܳ������������⣬��һ��Ҫ������_______________________ ��
��4����Ӧ������D�е������� ��
��5����B�з���������������л�����һ�������Ҵ������Ѻ�ˮ��Ӧ�ȼ�����ˮ�Ȼ��ƣ����˷���� ���ټ��루�˿մ�����ѡ����ѡ�� ��Ȼ����������ռ�77�����ҵ���֣��Եõ��ϴ���������������
A ���������� B ��ʯ�� C ��ˮ������ D ��ʯ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com