
用NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )。
| A.标准状况下,22.4 L CHCl3中含有的氯原子的数目为3NA |
| B.7 g CnH2n中含有的氢原子数目为NA |
| C.18 g D2O中含有的质子数目为10NA |
| D.0.5 mol·L-1 Na2CO3溶液中含有的CO32-的数目为0.5NA |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
NA代表阿伏加德罗常数,下列说法中正确的是
| A.标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA |
| B.密闭容器中,0.1 mol H2和25.4 g碘在一定条件下充分反应,生成HI分子数为0.2 NA |
| C.含有4 NA个碳碳σ键的金刚石,其质量为24 g |
| D.含0.1 mol FeCl3的溶液完全水解后得到的胶体粒子个数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
| A.3.2 g | B.4.0 g | C.4.2 g | D.4.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA为阿伏加德罗常数的值,下列叙述错误的是( )。
| A.18 g H2O中含有的质子数为10NA |
| B.12 g金刚石中含有的共价键数为4NA |
| C.46 g NO2和N2O4混合气体中含有原子总数为3NA |
| D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )。
| A.通入标准状况下的HCl气体11.2V L |
| B.加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L |
| C.将溶液加热浓缩到0.5V L |
| D.加入V L 1.5 mol·L-1的盐酸混合均匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设NA表示阿伏加德罗常数的值。下列叙述正确的是( )。
| A.42 g C3H6中含有的共用电子对数目为8 NA |
| B.电解饱和食盐水时,当0.1 mol NaCl反应时,转移的电子数为0.1 NA |
| C.常温常压下,22.4 L N2和O2的混合气体中含有的分子数目为NA |
| D.1 L 0.01 mol·L-1 KAl(SO4)2溶液中含有的阳离子数目为0.02 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为ρ g·cm-3。该盐酸的物质的量浓度、溶质的质量分数分别为( )。
A.c=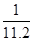 mol·L-1、w= mol·L-1、w=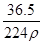 % % |
B.c=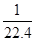 mol·L-1、w= mol·L-1、w=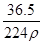 % % |
C.c=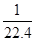 mol·L-1、w= mol·L-1、w=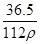 % % |
D.c=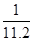 mol·L-1、w= mol·L-1、w=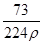 % % |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒
蒸发醋中的水分,以提高醋的品质。假设用含醋酸质量分数为3%的半成醋,生产500 g 0.945 mol·L-1的优级醋(密度为1.050 g·mL-1),生产过程中醋酸没有损失,捞出的冰和蒸发的水的总质量为( )
| A.100 g | B.200 g |
| C.300 g | D.400 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com