
| A������������Һ�м������������Һ��Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2O |
| B���Ȼ�����Һ�м��������ˮ��Al3++ 3 NH3��H2O = Al(OH)3�� + 3 NH4+ |
| C�����������Һ��ͨ������Ķ�����̼��Ca2+ +2ClO��+ H2O + CO2 = CaCO3��+ 2HClO |
| D���ڰ�ˮ��ͨ�������Ķ�������Ӧ��NH3��H2O + SO2 = NH4+ + HSO3�� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ȼ�����Һ��ʴͭ����Fe 3++ Cu �� Fe��++ Cu2+ |
| B��NaHCO3��Һ��NaOH��Һ��Ӧ��OH��+ HCO3���� CO2 ��+ H2O |
C����ⱥ��ʳ��ˮ��2Cl����2H2O 2OH����H2����Cl2�� 2OH����H2����Cl2�� |
| D��SO2ͨ�������İ�ˮ�У�SO2 + NH3 + H2O ="=" NH4+ + HSO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��̼��������ᷴӦ��2H+ + CO32��="=" CO2��+ H2O |
| B������ͭ������������Һ��Ӧ��Ba2+ + SO42�� ="=" BaSO4�� |
| C������ϡ���ᷴӦ��Fe + 2H+ ="=" Fe2+ + H2�� |
| D������������ˮ��Ӧ��SO2 + H2O ="=" 2H+ + SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ����������������Һ��ӦH����OH����H2O |
| B������ϡ���ᷴӦAl��2H����Al3����H2�� |
| C�����Ȼ�����Һ������������Һ��ӦFeCl3��3OH����Fe(OH)3����3Cl�� |
| D��������̼�����ʯ��ˮ��ӦCO2��2OH����CO32����H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
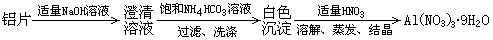 ��
��| A��2Al+2OH��+2H2O=2AlO2��+3H2�� | B��HCO3��+AlO2��+H2O=CO2��+Al(OH)3�� |
| C��NH4++AlO2��+2H2O=NH3��H2O+ Al(OH)3�� | D��3H++Al(OH)3=Al3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������ʵ���֮��Ϊ2��7�����Ȼ�����Һ������������Һ��� 2Al3+ + 7OH��= Al(OH)3 �� + AlO2��+ 2H2O |
| B�����������ʵ���֮��Ϊ4��3���������ƺ�����������Һ����Һ��ϣ� 4H����3SO42����3Ba2����4OH����3BaSO4����4H2O |
| C����ʯī�缫���⻯þ��Һ 2 I���� 2 e�� =" I" 2 |
| D����16.8g����Ͷ��100mL 4.0mol/L��HNO3��Һ�У���ԭ����ֻ��NO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ���������������Һ��Ӧ��H+ + OH��= H2O |
B��������ͭ��Һ�м�������������Һ Ba2����SO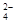 =BaSO4�� =BaSO4�� |
| C��������Ͷ��ˮ�� 2Na + 2H2O = 2Na+ + 2OH��+ H2�� |
| D������ͨ���廯����Һ�� Cl2��2Br�� = 2Cl����Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaHCO3=Na+ + H+ + CO32- | B��NaHSO4=Na+ + HSO4- |
| C��CH3COOH=CH3COO- +H+ | D��Na2SO4=2Na+ + SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʯ��ʯ�������CaCO3+2H+�T�T Ca2++H2O+ CO2�� |
| B����ˮ�μӵ��Ȼ�������Һ�У�Fe2++Cl2 �T�T Fe3++2Cl- |
| C����������ͭ��Һ��Ӧ��Fe+Cu2+�T�T Fe2++Cu |
| D��ϡ���������������Һ��ϣ�H++OH-�T�T H2O |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com