
| A. | 六水氯化钙属于混合物 | B. | 葡萄糖注射液不能产生丁达尔效应 | ||
| C. | 食盐水属于浊液 | D. | 氯化铵不属于盐类 |
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
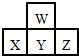 如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )| A. | 原子半径的大小顺序是Z>Y>X>W | |
| B. | Z的气态氢化物比X的气态氢化物稳定 | |
| C. | X、Y、Z各元素最高价和最低价的绝对值之和为8 | |
| D. | X、Y、Z最高价氧化物对应水化物的酸性强弱关系Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
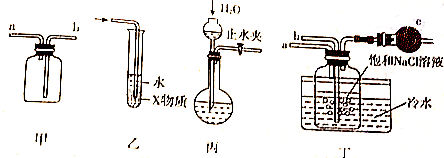
| A. | 装置甲可用于收集H2、NH3、CO2、Cl2等气体 | |
| B. | 装置乙中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 | |
| C. | 装置丙可以用于检验装置气密性 | |
| D. | 装置丁中b通入CO2,然后a通入NH3,用于实验室模拟制备NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入试剂 | 对应化学或离子方程式 | ||
| A | 乙烷(乙烯) | 氢气 | CH2=CH2+H2$→_{加热}^{Ni}$CH3CH3 |
| B | CH3COOC2H5(CH3COOH) | NaOH溶液 | CH3COOH+NaOH=CH3COONa+H2O |
| C | MgCl2( FeCl3) | 氨水 | Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ |
| D | Fe2+(Fe3+) | Fe粉 | 2Fe3++Fe=3Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 待测液 | 消耗标准盐酸(0.1000mol/L)的体积 | |
| ① | 20.00mL NaOH溶液 | V1 mL |
| ② | 20.00mL NaOH溶液+10.00mL水 | V2 mL |
| ③ | 敞口隔夜放置的20.00mL NaOH溶液 | V3 mL |
| A. | c=0.1000×$\frac{{V}_{1}+{V}_{2}+{V}_{3}}{3×20.00}$ | B. | c=0.1000×$\frac{{V}_{1}+{V}_{2}}{2×20.00}$ | ||
| C. | c=0.1000×$\frac{{V}_{1}+{V}_{3}}{2×20.00}$ | D. | c=$\frac{0.1000{V}_{1}}{20.00}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
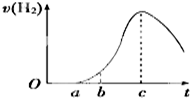 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示.
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com