
解释下列事实的方程式书写正确的是( )
A.加热可增强纯碱溶液去污力:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
B.用稀硝酸洗涤做过银镜反应的试管:Ag + 4H+ +NO3— = Ag++ NO↑++2H2O
C.向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+ O2+2SO2=2CO2+2CaSO4
D.碳酸氢钠溶液与少量澄清石灰水混合:HCO3-+Ca2++OH-=CaCO3↓+H2O
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一10月月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A.标准状况下,22.4 L H2O含有的分子数为NA个
B.常温常压下,1.06 g Na2CO3含有的Na+数为0.02 NA个
C.1 mol OH一中含有9 NA个电子
D.物质的量浓度为0.5 mol·L-1的MgCl2溶液中,含有Cl-个数为NA个
查看答案和解析>>
科目:高中化学 来源:2016届辽宁沈阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
已知M、Q、X、Y、Z是前四周期中元素(不包含稀有气体元素),有关性质和相关信息如下表:
元素 | 相关信息 |
M | 最高价氧化物对应的水化物能按1:1电离出电子数相等的阴、阳离子 |
Q | 所在主族序数与所在周期序数之差为4,非金属性在同周期元素中最强 |
X | 其单质为淡黄色晶体 |
Y | 某种核素原子的质量数为56,中子数为30 |
Z | X元素的单质在Z元素的单质中燃烧,发出明亮的蓝紫色火焰 |
(1)下图是不完整的元素周期表,补全元素周期表的轮廓,并将Y的元素符号填在元素周期表中相应的位置上。
(2)M与Z形成的含有共价键的化合物的电子式为 。
(3)M、Q、Z简单离子的半径由大到小的顺序为 (用离子符号表示)。
(4)用一个化学方程式表示证明非金属性Q>X: 。
(5)5.6L标准状况下的X的简单氢化物在足量的Z单质中完全燃烧生成液态水时,放出的热量为356.8kJ。该反应的热化学方程式为 。
(6)在碱性条件下,Q的单质可与YZ2-反应制备一种可用于净水的盐YZ42-,该反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:选择题
700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)。反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | H2O/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是( )
A.反应在t1 min内的平均速率为v(H2)= mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,到达平衡时n(CO2)=0.30 mol
C.保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升高至800 ℃, 上述反应平衡常数为0.64,则正反应为吸热反应
上述反应平衡常数为0.64,则正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2016届河北正定中学高三上学期期中考试化学试卷(解析版) 题型:选择题
某化学研究性学习小组对电解质溶液作出如下的归纳总结(均在常温下),其中正确的是( )
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度一定降低
②pH=2的盐酸和pH=1的盐酸,c(H+) 之比为2:1
之比为2:1
③pH相等的四种溶液:a.CH3COONa、b.C6H5ONa、c.NaHCO3、d.NaOH。其溶液物质的量浓度由小到大的顺序为d、b、 c、a
c、a
④NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO42-)
⑤已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则三者关系为Ka·Kh=Kw
⑥甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙两溶液等体积混合,混合液pH可能等于7
A.③④⑥ B.③⑤⑥ C.④⑤⑥ D.①②④
查看答案和解析>>
科目:高中化学 来源:2016届湖南长沙市三上学期第四次月考化学试卷(解析版) 题型:简答题
(1)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.100 0mol·L-1CH3COOH溶液所得滴定曲线如下图。已知起始①点溶液的pH为3,③点溶液的pH为7,则Ka(CH3COOH)=____________。

(2)在用Na2SO3溶液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
0.01mol·L-1Na2SO3溶液中通人SO2至溶液呈中性时,溶液中的所有离子的浓度由大到小的顺序是___________________。
(3)向0.1mol·L-1的NaHSO3中通人氨气至溶液呈中性时,溶液中的c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系是____________________。
(4)已知Ca3(PO4)2、CaHPO4均难溶于水,而Ca(H2PO4)2易溶,在含0.1molCa(OH)2的澄清石灰水中逐滴加入1mol·L-1的H3PO4,请作出生成沉淀的物质的量随H3PO4滴人体积从0开始至200mL的图像。

查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三12月月考化学试卷(解析版) 题型:实验题
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
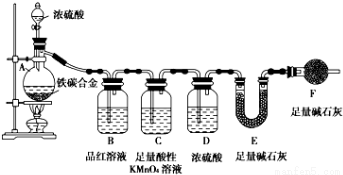
I.探究该合金的某些性质:
(1)取a g合金粉末放人蒸馏烧瓶,并加入足量浓H2SO4,A、B中均无明显现象,原因是_______;
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出此时合金中成分铁的化学反应方程式_____;
(3)反应一段时间后,将C中所吸收的气体通入以下溶液中,判断能否产生沉淀,若不能则写“否”,若能则写出相应的沉淀成分:氯水和氯化钡溶液____,氨水和氯化钡溶液_____;
II.测定样品中碳的质量分数:
(4)装置F的作用__________________________________________________________;
(5)若将SO 2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海西宁第十四中学高二上期中考试化学卷(解析版) 题型:填空题
室温下将pH=13的强碱溶液和pH=2的强酸溶液混合,所得溶液的pH=12,则强碱溶液和强酸溶液的体积之比为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安第一中学高二上期中考试化学试卷(解析版) 题型:填空题
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的由线如图所示。请回答:
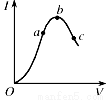
(1)“O”点导电能力为O的理由是 。
(2)a,b,c三点溶液中 c(H+)由小到大的顺序为 。
(3)a,b,c三点中电离程度最大的是 。
(4)使C点溶液中C(CH3COO-)增大,溶液c(H+)减小,可采取的
措施是:① ② ③  (至少填两个空)
(至少填两个空)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com