
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构, 且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
分析 由A单质是密度最小的物质,可知A为H;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O;C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,则C为Na;D的氢氧化物和氧化物都有两性,与C同周期,则D为Al;E与C同周期,原子半径在该周期最小,则E为Cl,以此来解答.
解答 解:由A单质是密度最小的物质,可知A为H;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O;C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,则C为Na;D的氢氧化物和氧化物都有两性,与C同周期,则D为Al;E与C同周期,原子半径在该周期最小,则E为Cl,
(1)由上述分析可知,B、C、D、E分别为氧(O)、钠(Na)、铝(Al)、氯(Cl),
故答案为:氧(O);钠(Na);铝(Al);氯(Cl);
(2)C与B形成的两种离子化合物的化学式为Na2O、Na2O2,故答案为:Na2O、Na2O2;
(3)实验测得DE3在熔融状态下不导电,由分子构成,不含离子键,则DE3中含有的化学键类型为共价键,故答案为:共价键.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素化合物性质推断元素为解答的关键,侧重分析与应用能力的考查,注意离子化合物、共价键等判断,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 晶体类型 | 离子晶体 | 原子晶体 | 分子晶体 |
| 各组中物质的编号 | ①④ | ②⑤ | ③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
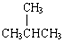 ;④CH4与C3H8;⑤CH3CH2CH2CH3与
;④CH4与C3H8;⑤CH3CH2CH2CH3与 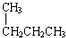 .请回答下列问题:
.请回答下列问题: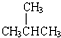 的名称是2-甲基丙烷.
的名称是2-甲基丙烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③→⑧→①←④→⑨ | B. | ⑦→③→⑥→①←④→⑨→② | C. | ②→⑨→④→①←⑥←③ | D. | ②→④→⑤→①←⑥←③ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
. .
. 与过量的
与过量的 也可以发生Reformatsky反应,试写出该生成物的结构简式
也可以发生Reformatsky反应,试写出该生成物的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com