
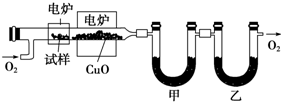
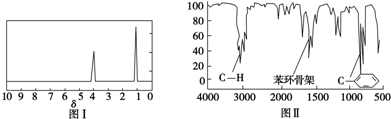
���� ��1����X�����ʵ���Ϊ$\frac{2.12g}{106g/mol}$=0.02mol�����ɶ�����̼Ϊ$\frac{7.04g}{44g/mol}$=0.16mol������ˮΪ$\frac{1.8g}{18g/mol}$=0.1mol���������N��C��=$\frac{0.16mol}{0.02mol}$=8��N��H��=$\frac{0.1mol��2}{0.02mol}$=10����X�ķ���ʽΪC8H10��X�ĺ�����ײⶨ���б��������ڱ���ͬϵ���1H�˴Ź�������2���壬�����֮��Ϊ2��3����XΪ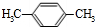 ��
��
��2��ͨ��������������Է��������ķ���Ϊ������
��� �⣺��1������X�����ʵ���Ϊ$\frac{2.12g}{106g/mol}$=0.02mol�����ɶ�����̼Ϊ$\frac{7.04g}{44g/mol}$=0.16mol������ˮΪ$\frac{1.8g}{18g/mol}$=0.1mol���������N��C��=$\frac{0.16mol}{0.02mol}$=8��N��H��=$\frac{0.1mol��2}{0.02mol}$=10����X�ķ���ʽΪC8H10��X�ĺ�����ײⶨ���б��������ڱ���ͬϵ���1H�˴Ź�������2���壬�����֮��Ϊ2��3����XΪ ������Ϊ�Զ��ױ���
������Ϊ�Զ��ױ���
�ʴ�Ϊ��C8H10���Զ��ױ���
��2�������ͨ������������֪X����Է����������÷�����Ϊ������
�ʴ�Ϊ��������
���� ���⿼���л�����ƶϡ���������ͬ���칹����д��ע���л����о���һ�㷽���벽�裬�Ѷ��еȣ����ؿ���ѧ���ķ��������ͼ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
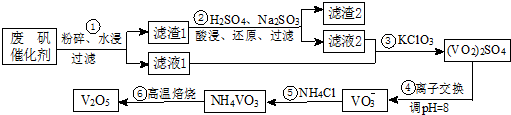
| ���� | VOSO4 | V2O5 | NH4VO3 | ��VO2��2SO4 |
| �ܽ��� | ���� | ���� | ���� | ���� |
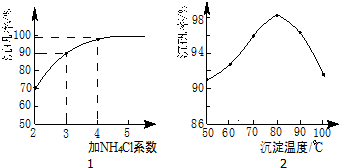
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
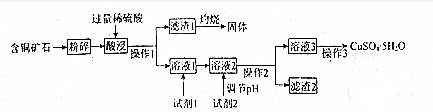
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��2 | 7.6 | 9.6 |
| Fe��OH��3 | 2.7 | 3.7 |
| Cu��OH��2 | 4.0 | 6.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
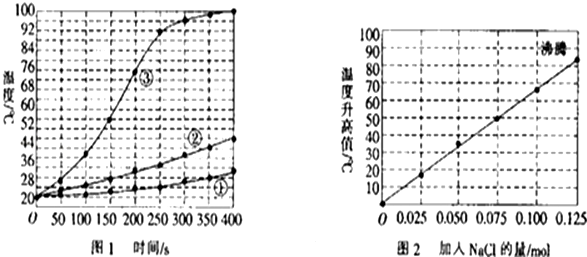
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O��g��=H2O��l����H=-44kJ/mol�����Ըù����Ƿ��ȷ�Ӧ | |
| B�� | �������õ���Դ����ͨ����ѧ��Ӧ��õ� | |
| C�� | 2CO��g��+O2$\frac{\underline{\;��ȼ\;}}{\;}$2CO2��g����H��0����56gCO��32gO2�����е����������88g�����е������� | |
| D�� | ��Ҫ���ȵķ�Ӧһ�������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�� | B�� | ���� | C�� | ���� | D�� | Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 21% | B�� | 25% | C�� | 30% | D�� | 35% |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com