
 ����Ӧ���ͣ��Ӿ۷�Ӧ
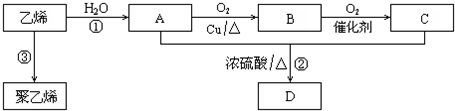
����Ӧ���ͣ��Ӿ۷�Ӧ���� C2H4�����Ӿ۷�Ӧ�õ�����ϩ����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������ӦCH3CHO��BΪCH3CHO��CH3CHO�ɽ�һ��������CH3COOH��CΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����CH3COOCH2CH3����DΪCH3COOCH2CH3���ݴ˷������
��� �⣺C2H4�����Ӿ۷�Ӧ�õ�����ϩ����ϩ��ˮ�����ӳɷ�Ӧ����AΪCH3CH2OH���Ҵ���Cu��Ag�����������·���������ӦCH3CHO��BΪCH3CHO��CH3CHO�ɽ�һ��������CH3COOH��CΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����CH3COOCH2CH3����DΪCH3COOCH2CH3��
��1��ͨ�����Ϸ���֪��BΪCH3CHO��A��C��ԭ���ŷֱ�Ϊ�ǻ����Ȼ���
�ʴ�Ϊ��CH3CHO���ǻ����Ȼ���
��2���ٸ÷�ӦΪ�ʴ�Ϊ��CH2�TCH2+H2O$\stackrel{һ��������}{��}$CH3CH2OH��Ϊ�ӳɷ�Ӧ��
��Ϊ��ϩ�ļӾ۷�Ӧ����Ӧ����ʽΪ ��Ϊ�Ӿ۷�Ӧ������ϩ�ĵ�����CH2�TCH2��
��Ϊ�Ӿ۷�Ӧ������ϩ�ĵ�����CH2�TCH2��
�ʴ�Ϊ��CH2�TCH2+H2O$\stackrel{һ��������}{��}$CH3CH2OH���ӳɷ�Ӧ��  ���Ӿ۷�Ӧ��CH2�TCH2��
���Ӿ۷�Ӧ��CH2�TCH2��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ���������ȷ�����ż������ʹ�ϵ������֮���ת������Ӧ��������Ӧ�����ж��ǽⱾ��ؼ�����Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| �𡡡��� | �۵㣨�棩 | �е㣨�棩 |
| �� | 841 | 1 487 |
| �� | 920 | 3 470 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

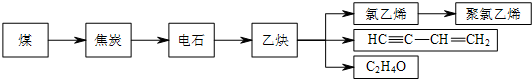
 �����ⶪ��������ϩ��Ʒ����ɰ�ɫ��Ⱦ��
�����ⶪ��������ϩ��Ʒ����ɰ�ɫ��Ⱦ��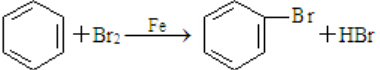 ���÷�Ӧ�з�Ӧ����Ӧ��ѡ��Һ�壨���ˮ����Һ�塱����
���÷�Ӧ�з�Ӧ����Ӧ��ѡ��Һ�壨���ˮ����Һ�塱�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��NaOH | B�� | H2��Al��OH��3 | C�� | H2��NaCl��NaAlO2 | D�� | H2��NaCl��Al��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ը��������Һ�����������ϩ | |
| B�� | ��BaCl2��ȥNaOH ��Һ�л��е�����Na2SO4 | |
| C�� | ��KSCN��Һ������Һ�к��е�Fe2+ | |
| D�� | ���ܽ⡢���˵ķ�������CaCl2��NaCl�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������� | B�� | ���������ڱ���ˮ�� | ||
| C�� | ʯ�����������ģ�� | D�� | ̼����刺��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ��ʯ������ | B�� | ̼����狀����� | C�� | ̼��غʹ��� | D�� | ̼���ƺ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
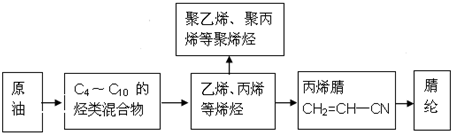
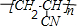 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���з�̪�İ�ˮ�м�������NH4Cl���壬��Һ��ɫ��dz | |
| B�� | ��Ũ�ȵ�С�մ���Һ���ռ���Һ�������ϣ�c��Na+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-�� | |
| C�� | ��pH=12��NaOH��Һ�еμ�pH=2��HA��Һ�����ԣ������V��HA����V��NaOH�� | |
| D�� | ��֪298Kʱ�����ᣨHCN����Ka=4.9��10-10��̼���Ka1=4.4��10-7��Ka2=4.7��10-11���ݴ˿��Ʋ⽫��������뵽̼������Һ���ܹ۲쵽�����ݲ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com