
| A. | 会引起化学键的变化 | B. | 必然引起物质状态的变化 | ||
| C. | 必然伴随着能量的变化 | D. | 会产生新的物质 |
科目:高中化学 来源: 题型:选择题
| A. | 将金属K放在烧杯中燃烧,火焰呈紫色 | |
| B. | 非极性键只存在于双原子的单质分子(如Cl2)中 | |
| C. | 原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 | |
| D. | 由不同元素组成的含多个原子的分子里,一定只存在极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 的同分异构体中同时符合下列条件的芳香族化合物共有6种.
的同分异构体中同时符合下列条件的芳香族化合物共有6种. (任写一种)(任写一种).
(任写一种)(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
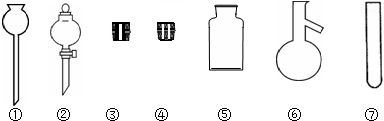
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,CH(CH3)3的名称为:2-甲基丙烷.
,CH(CH3)3的名称为:2-甲基丙烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 解释或结论 |
| A | 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 | 反应物的浓度一定降低 |
| B | 压缩针筒内的NO2和N2O4混合气体,颜色先变深后变浅 | 增大压强,平衡向生成N2O4的方向移动 |
| C | 由水电离出来的c(H+)=1.0×10-13mol/L溶液 | 该溶液为氯化铵水溶液 |
| D | 向含有NH4+、Mg2+、Cu2+、Al3+溶液中加入过量的氢氧化钠溶液微热并搅拌,再加过量的盐酸,其中NH4+大量减少 | NH4+水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
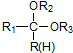 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$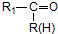
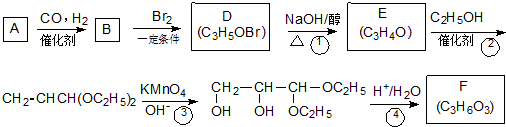
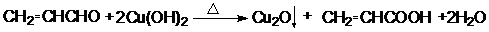 ;
;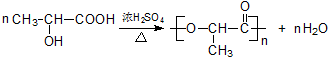 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 0.1mol/L的FeCl3溶液 | B. | 20mL 0.1mol/L的MgCl2溶液 | ||
| C. | 30mL 0.2mol/L的KCl溶液 | D. | 100mL 0.25mol/L的HCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com