
【题目】应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知:①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) ΔH=-38.19 kJ·mol-1
则表示 CH3OH的燃烧热的热化学方程式为___________ 。
(2)在一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g) ![]() CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:
CH3OH(g),在2 L恒容密闭容器中充入1 mol CO和2 mol H2,在催化剂作用下充分反应。 上图表示平衡混合物中 CH3OH的体积分数在不同压强下随温度的变化的平衡曲线。回答下列问题:

①该反应的反应热 ΔH________ 0(填“>”或“<”), 在_______ (填“高温”、“低温” )下易自发,压强的相对大小与 p1_______ p2(填“>”或“<”)。
②压强为 p2,温度为300℃时,该反应的化学平衡常数的计算表达式为 K=_______。
③下列各项中,不能说明该反应已经达到平衡的是_______。
A.容器内气体压强不再变化 B.υ(CO):υ(H2)=1:2
C.容器内的密度不在变化 D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
④某温度下,在保证 H2浓度不变的情况下,增大容器的体积,平衡_______。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
【答案】 CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.51 kJ·mol-1 < 低温 > ![]() BC C
BC C
【解析】(1)已知:①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH1=+93.0 kJ·mol-1;
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH2=-192.9 kJ·mol-1;
③CH3OH(g)=CH3OH(l) ΔH3=-38.19 kJ·mol-1;根据盖斯定律可知,②×3-①×2-③得反应CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ,此时 ΔH=(-192.9 kJ·mol-1)×3-(+93.0 kJ·mol-1)×2-(-38.19 kJ·mol-1)=-726.51 kJ·mol-1;即CH3OH的燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.51 kJ·mol-1;
O2(g)=CO2(g)+2H2O(l) ,此时 ΔH=(-192.9 kJ·mol-1)×3-(+93.0 kJ·mol-1)×2-(-38.19 kJ·mol-1)=-726.51 kJ·mol-1;即CH3OH的燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.51 kJ·mol-1;
(2)①由图可知,升高温度,CH3OH的体积分数减小,平衡逆向移动,则该反应的△H<0;已知CO(g)+2H2(g) ![]() CH3OH(g)的△S<0,根据△G=△H-T△S,当反应处于低温时,△G<0,反应能自发进行;300℃时,增大压强,平衡正向移动,CH3OH的体积分数增大,所以p1>p2;
CH3OH(g)的△S<0,根据△G=△H-T△S,当反应处于低温时,△G<0,反应能自发进行;300℃时,增大压强,平衡正向移动,CH3OH的体积分数增大,所以p1>p2;
②压强为 p2,温度为300℃时,平衡混合物中 CH3OH的体积分数为50%,
CO(g) + 2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始物质的量浓度(mol/L) 0.5 1 0
变化的物质的量为浓度(mol/L) c 2c c
平衡的物质的量为浓度(mol/L) 0.5-c 1-2c c
则:![]() =50%,解得:c=0.375,则该反应的化学平衡常数的计算表达式为 K=
=50%,解得:c=0.375,则该反应的化学平衡常数的计算表达式为 K=![]() =
=![]() ;
;
③A.随反应进行混合气体物质的量减小,恒温恒容下压强减小,容器中压强保持不变说明到达平衡,故A错误;B.伴随反应的进行过程中,始终保持υ(CO):υ(H2)=1:2,则不能说明反应到达平衡,故B正确;C.混合气体总质量不变,恒温恒容下,容器内气体密度始终保持不变,不能说明反应到达平衡,故C正确;D.混合气体总质量不变,随反应进行混合气体物质的量减小,平均相对分子质量增大,平均相对分子质量不变说明到达平衡,故D错误;E.容器内各组分的质量分数不再变化说明到达平衡,故E错误;故答案为BC;
④某温度下,在保证H2浓度不变的情况下,增大容器的体积,说明c(CH3OH)与c(CO)同等倍数减小,又浓度商Qc=![]() =K,此时平衡不移动,故答案为C。
=K,此时平衡不移动,故答案为C。


科目:高中化学 来源: 题型:
【题目】使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应,则消耗的氯气的总的物质的量是
A. 3mol B. 4mol C. 5mol D. 6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙.
【查阅资料】
Ⅰ.金属Ca的部分性质有:
①常温或加热条件下Ca都能与氧气反应;
②Ca常温遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热;
③Ca+H2 ![]() CaH2(固体)
CaH2(固体)
Ⅱ.固体CaH2的部分性质有:
①常温:CaH2+2H2O=Ca(OH)2+2H2↑; ②CaH2要密封保存.
(1)【进行实验】
该小组同学设计的制取装置如图所示(固定装置略).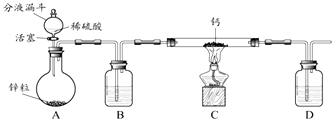
回答下列问题:
(i)写出Ca常温遇水发生反应的化学方程式: .
(ii)B、D中所盛试剂相同,该试剂为(填名称);D中该试剂的作用是 .
(iii)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是: .
(2)【实验反思】
该小组同学通过反思提出问题:上述制得的CaH2是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量为m g的CaH2样品,按图所示连接仪器(固定装置略).
步骤2:将Y形管倾斜,使A中的水全部进入B中,样品全部反应后,冷却至室温,读取量筒读数为V mL.
(iv)若该实验条件下的气体摩尔体积为Vm L/mol,当V=mL时(用m、Vm表示),表明制得的CaH2样品是纯净的.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述中正确的是( )
A. 常温下64 g S4和S8混合物中含有原子数为2NA
B. 标准状况下,22.4LHF中含电子数为10NA
C. l L1 mol/L的盐酸溶液中,所含氯化氢分子数为NA
D. 足量铁在1mol氯气中加热反应,铁失去的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年8月7日,PLOS Biology在线发表了关于玉米生物固氮的研究,为减少化肥使用和发展绿色农业提供重要的理论指导,固氮通常指将氮元素从游离态转化为化合态的过程。下列变化属于固氮的是
A.NH3→NOB.N2 → NH3
C.NO →NO2D.NO2→HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃ 时纯水的电离度α1,pH=11的氨水中水的电离度为α2,pH=3的盐酸中水的电离度α3.若将上述氨水与盐酸等体积混合,所得溶液中的电离度为α4下列关系式中正确的是
A.α1<α2<α3<α4B.α3=α2<α1<α4
C.α2<α3<α1<α4D.α2=α3<α4<α1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能说明苯与一般的烯烃性质不同的事实是( )
A. 苯分子是高度对称的平面型分子
B. 苯能燃烧
C. 苯不与酸性KMnO4溶液反应
D. 1mol苯在一定条件下可与3 mol氯气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃烧电池原理示意图,按照此图的提示,下列叙述正确的是( )

A. a电极是正极
B. b电极的电极反应为:4OH-- 4e-=2H2O + O2↑
C. 电子从a电极经由电解液传递到b电极
D. 氢氧燃烧电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com