
【题目】下列有关反应的能量变化,错误的是
A.化学反应中,有放热反应也有吸热反应
B.化学反应中的能量变化主要是由化学键的变化引起的
C.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应是放热反应
D.盐酸与NaOH溶液的反应是放热反应
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法,错误的是( )
A. 乙酸乙酯在一定条件下可以水解成乙醇和乙酸
B. 油脂和蔗糖都属于高分子化合物
C. 油脂水解能得到甘油
D. 淀粉、纤维素在一定条件下水解均可得到葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3,方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
据以上信息回答下列问题:
a.用稀盐酸浸取炉渣,过滤,除掉的杂质为 。
b.除去Al3+的离子方程式是 。
c.选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂:稀盐酸 稀硫酸 KSCN溶液KMnO4溶液NaOH溶液所选试剂为 。证明炉渣中含有FeO的实验现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对SO2的性质描述不正确的是
A. 无色、有刺激性气味的气体
B. 和水反应生成硫酸
C. 有漂白性,能使品红溶液褪色
D. 具有还原性,能被氧气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组的离子,能在溶液中大量共存的是
A. K+、H+、SO42-、OH- B. Na+、 Ca2+、 CO32-、NO3-
C. Na+、H+、Cl-、CO32- D. Na+、 Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是

A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在隔绝空气的装置中,将0.2mol铁和铝的混合物溶于400ml c(H+)为2mol/L稀硫酸中,然后滴加1mol/L的NaOH溶液,请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液的体积的变化如图所示。
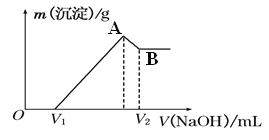
A点时溶液中的溶质有 ;此时溶液刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= 。当V1=300ml时,金属粉末中n(Fe)= mol,V2= ml.
(2)写出AB段有关的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
I.喷泉是一种常见的自然现象,其产生的原因是存在压强差。
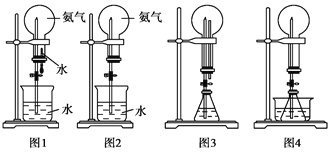
(1)实验室制取氨气的化学方程式____ __。
①用图1装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是___________。
②如果只提供如图2的装置, (“能”或“不能”)实现喷泉实验
(2)利用图3装置,在锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是________。
A.Cu与稀盐酸 B.NaHCO3溶液与NaOH溶液
C.CaCO3与稀H2SO4D.NH4HCO3与稀盐酸
(3)在图4锥形瓶中加入酒精,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是________。
A.浓硫酸 B.食盐
C.硝酸钾 D.硫酸铜

(4)从产生喷泉的原理分析,图 是减小上部烧瓶内的压强。图 是增大下部锥形瓶内气体的压强。人造喷泉及火山爆发的原理与上述装置图________原理相似。(均填序号)
II.某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置。
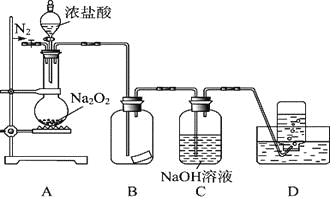
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接仪器。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)装置B中的湿润的红色纸条褪色,证明A中反应有 (填化学式)生成。若B中改放湿润的淀粉KI试纸,仅凭试纸变蓝的现象不能证明上述结论,请用离子方程式说明原因 。
(2)装置C的作用是 。
(3)甲同学认为O2是Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,他可能的理由为
① ;② 。
(4)实验证明,Na2O2能与干燥的HCl反应,完成并配平该化学方程式。
Na2O2 + HCl ----- Cl2 + NaCl +
该反应 (填“能”或“不能”)用于实验室快速制取纯净的Cl2,理由是 (要求答出一个要点即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com