
MnO2是具有多种特殊功能的材料,工业上用菱铁矿(MnCO3)为原料制备MnO2的工业流程如下:
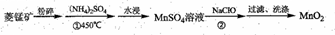
试回答以下问题:
(1)提高水浸效率的方法有______、______(填两种)。实验室里洗涤MnO2时用到的玻璃仪器有_____。NaClO的电子式为_________。
(2)反应①的化学方程式为___________。
(3)反应②生成MnO2的同时,得到一种黄绿色的气体,则该反应的离子方程式为__________。
(4)反应②的尾气常温下通入NaOH溶液后,生成NaClO可循环利用,若制得87gMnO2,理论上还需要补充NaClO______mol。
(5)工业上还可以将菱锰矿用硫酸直接浸取后,通过电解MnSO4和H2SO4的混合液制备MnO2,则电解时阳极的电极反应式为__________。
科目:高中化学 来源:2015-2016学年江西省高二上二次月考化学试卷(解析版) 题型:实验题
用中和滴定的方法测定NaOH和Na2CO3的混合溶液中NaOH的含量,可先在混合液中加入过量的BaCl2溶液,使Na2CO3完全转变成BaCO3沉淀,然后用标准盐酸滴定(已知几种酸碱指示剂变色的pH范围:①甲基橙3.1~4.4 ②甲基红4.4~6.2 ③酚酞8.2~10)。
(1)滴定时应选用 作指示剂;
(2)判断到达滴定终点的实验现象是 。
(3)下列操作会导致烧碱样品中NaOH含量测定值偏高的是
A.锥形瓶用蒸馏水洗后未用待测液润洗 B.酸式滴定管用蒸馏水洗后未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失 D.滴定前平视读数,滴定结束俯视读数
(4)为测定某烧碱样品中NaOH的含量(设样品中杂质为Na2CO3),某同学进行如下实验:准确称取5.0g样品配制成250mL溶液,然后分三次各取配制好的烧碱溶液20.00mL于三个用蒸馏水洗净的锥形瓶中,分别加入过量的BaCl2溶液,并向锥形瓶中各加入1~2滴指示剂,用浓度为0.2000mol·L-1的盐酸标准液进行滴定,相关数据记录如下:
实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
初读数 | 末读数 | ||
1 | 20.00 | 0.80 | 21.00 |
2 | 20.00 | 1.00 | 20.80 |
3 | 20.00 | 0.20 | 22.80 |
依据表中数据,计算出烧碱样品中含NaOH的质量分数为 %。(小数点后保留两位数字)
(5)若某样品可能由NaOH、Na2CO3、NaHCO3中的一种或两种组成,为确定其组成,某同学进行下列实验:
准确称取mg样品配制成250mL溶液,取配制好的溶液20.00mL于锥形瓶中,加入2滴酚酞作指示剂,用浓度为cmol·L-1的盐酸标准液进行滴定至终点,消耗盐酸标准液v1ml,然后再滴加2滴甲基橙继续用浓度为cmol·L-1的盐酸标准液进行滴定至终点,消耗盐酸标准液v2ml(v1和v2均不为0),
根据v1和v2数值大小判断样品的组成(用化学式表示):
①v1>v2 ②v1=v2 ③v1<v2
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期12月月考化学试卷(解析版) 题型:选择题
“84”消毒液有效成分为 NaClO, 已知酸的电离平衡常数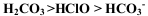 ,下列说法正确的是( )
,下列说法正确的是( )
A.“84”消毒液可以与福尔马林溶液混合使用
B.NaClO的稳定性和漂白性都比HClO强
C.工业上在特定条件下电解饱和食盐水制得NaClO,原理为:NaCl + H2O = NaClO +H2↑
D.NaClO溶液在空气中发生离子反应为: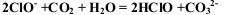
查看答案和解析>>
科目:高中化学 来源:2016届吉林长春外国语学校高三上第一次质检化学试卷(解析版) 题型:选择题
下列离子方程式正确的是 ( )
A.铝溶于烧碱溶液:Al+2OH-=AlO2-+H2↑
B.用铜电极电解硫酸铜溶液:2Cu2++ 2H2O 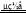 2Cu↓ +O2↑ +4H+
2Cu↓ +O2↑ +4H+
C.用FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水) Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
D.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液。当Pb(CH3COO)2溶液中通入H2S气体时有黑色沉淀生成:Pb2++H2S=PbS↓+2H+
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.MgO的熔点高,可用做防火板材料
B.BaC03与盐酸反应,可用于治疗胃酸过多
C.臭氧有强氧化性,可用于餐具消毒
D.NH3易液化,可用作制冷剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:计算题
现有m g某气体X2,它的摩尔质量为M g·mol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为____________________mol.
(2)该气体所含原子总数为_______________________个.
(3)该气体在标准状况下的体积为____________________L.
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为__________________.
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为__________________mol·L-1.
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
用惰性电极实现电解,下列说法正确的是 ( )
A.电解稀硫酸溶液,实质上是电解水,故溶液p H不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第三次月考化学试卷(解析版) 题型:选择题
—种直接肼燃料电池的结构如图所示,下列说法正确的是

A.a极为电池的正极
B.电路中每转移6.02X1023个电子,则有1molNa+穿过膜向正极移动
C.b极的电极反应式为H202+2e- 20H-
20H-
D.用该电池电解饱和食盐水,当阳极生成2.24 L(标准状况)Cl2时,消耗肼0.1 mol
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第三次模拟化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
①过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
②常温下21gC3H6和C4H8的混合物中含有的碳原子数为1.5 NA
③2L0.5mol/L亚硫酸溶液中含有的H+为2NA
④3mol单质铁完全转化为Fe3O4,失去8NA个电子
⑤密闭容器中2molNO与1molO2充分反应后,产物的分子数为2NA
⑥将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
A.①③⑤ B.④⑤⑥ C.①②④ D.①⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com