


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、室温时,0.1L 1mol?L-1的盐酸,溶液中水电离出的H+数为10-13NA | B、1L 0.2mol?L-1MgSO4溶液中的阳离子数小于0.2NA | C、2.88g ND2中含有的电子数是0.18NA | D、常温常压下,3g HCHO和CH3COOH混合物中含有0.4NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的N2和CO所含分子数均为NA | B、3.4gNH3中含N-H键数目为0.2NA | C、标准状况下的22.4L辛烷完全燃烧,生成CO2分子数为8NA | D、Na2O2与足量H2O反应生成0.2molO2,转移电子的数目为0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热反应后固体,投入足量稀硫酸溶液中,消耗硫酸物质的量为0.02mol | B、固体加热反应后,固体中还含氧化物物质的量0.05mol | C、反应的浓硝酸物质的量浓度为14mol/L | D、加热后固体与HNO3反应转移电子为0.36mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
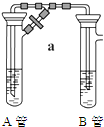 两同学为制得纯净的Fe(OH)2,使用如图所示的装置,A管中是Fe和H2SO4,B管中是NaOH溶液:
两同学为制得纯净的Fe(OH)2,使用如图所示的装置,A管中是Fe和H2SO4,B管中是NaOH溶液:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锌粒与盐酸反应时,若加入适量氯化钠晶体,可明显加快反应速率 | B、氯化钠中所含化学键为离子键,含离子键的化合物一定是离子化合物 | C、标准状况下,氯化钠溶液呈中性,溶液的pH=7 | D、氯化钠溶液导电是化学变化,而熔融态氯化钠导电是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、预防H7N9流感病毒的措施之一是高温消毒餐具等生活日用品 | B、《添加剂标准》中儿童膨化食品拟禁含铝添加剂,铝对人体有毒害 | C、我国京津冀等城市实施SO2、CO2、NO2、N2等大气污染物排放限值 | D、明矾、硫酸铁等在水中因水解生成胶体粒子,都可用作净水剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com