
【题目】下列反应中,水只表现出还原性的是
A. 2Na+2H2O=2NaOH+H2↑
B. 2F2+2H2O=4HF+O2
C. 3NO2+H2O=2HNO3+NO
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸溶液,B(OH)2、B(OH)+、B2+的浓度分数δ随溶液POH[POH=-lgc(OH)-]变化的关系如图,以下说法正确的是
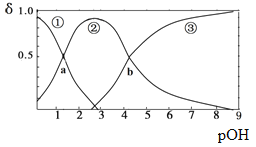
A. 交点a处对应加入的盐酸溶液的体积为5mL
B. 当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C. 交点b处c(OH)=6.4×10-5
D. 当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+),
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属A及其化合物之间有如下的转化关系:
(1)写出A、B的化学式:A_______,B_________。
(2)写出B→D的化学方程式_______________________________。
(3)写出B→C的离子方程式________________________________。
(4)写出E→C的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式_________________________________________________。
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为___________(填化学式)。在该溶液中加入___________试剂,看到_____________________现象,证明溶液变质。
(3)已知:Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是___________(填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,a点时,n(BaSO4)_____ n(Al(OH)3)(填“>”“<”“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若定义pAg=-lgc(Ag+),pCl=-1gc(C1-),根据不同温度下氯化银饱和溶液的PAg和pCl 可绘制图像如右图所示,且己知氯化银的溶解度随温度的升高而增大,根据该图像,下列表述正确的是

A. T3 >T2 >T1
B. 将A点的溶液降温,可能得到C 点的饱和溶液
C. 向B点所表示的溶液中加入氯化钠溶液,溶液可能改变至D点
D. A点表示的是T 1温度下的不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含有少量NaCl、Na2SO4、Na2CO3、泥沙(SiO2)等杂质的NaNO3固体,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
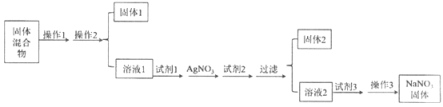
(1)操作1、操作3的名称分别是_________、_________。
(2)试剂1和试剂2分别是_________、_________。固体2中除了含有AgCl,还有_________(答全)。
(3)试剂3加入后发生的离子反应方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.0mL于锥形瓶中,加入10.0mL的KI溶液(足量),发生的反应为:Cl2+2KI=2KC1+I2,滴入指示剂2~3滴。
②取碱式滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol/LNa2S2O3溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6.试回答下列问题:
(1)步骤①加入的指示剂是____________。
(2)判断达到滴定终点的实验现象是____________。
(3)假设未描述的事项都规范合理,则该测定结果将_______(填“偏高”、“偏低”或“无影响”)。
(4)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11,草酸H2C2O4,K1=5.9X10-2,K2=6.4×10-5。0.1mol/LNa2CO3溶液的pH____0.1mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)。若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是________。(选填编号)
A. c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-) B. c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C. c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-) D. c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
(5) 已知: ①难溶电解质的溶度积常数: Ksp(CaF2)=1.5×10-10②25℃时,2.0×10-3mol/L氢氟酸水溶液中,调节溶液pH (忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示,请根据以下信息回答下列问题:

①25℃时,HF电离平衡常数的数值Ka≈________。
②4.0×10-3mo1/LHF溶液与4.0×10-4mo1/L CaCl2液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),请通过列式计算说明是否有沉淀产生:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是

A. 已知H3FeO4+的电离半衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pII=4吋,溶液中![]()
B. 为获得尽可能纯净的高铁酸盐,应控制pH≥9
C. 向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4ˉ+OHˉ=FeO42-+H2O
D. pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)> c (HFeO4ˉ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com