
【题目】下列关于平衡常数K的说法中,正确的是
A. 在任何条件下,化学平衡常数是一个恒定值
B. 改变反应物浓度或生成物浓度都会改变平衡常数K
C. 平衡常数K只与温度有关,与反应浓度、压强无关
D. 从平衡常数K的大小不能推断一个反应进行的程度
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】漂白粉可由Cl2通入消石灰中制备。漂白粉的有效成分是 ( )
A. Ca(OH)2 B. CaCl2 C. Ca(ClO)2 D. CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于原电池和电解池的叙述正确的是( )
A. 原电池中失去电子的电极为阴极
B. 原电池的负极、电解池的阳极都发生氧化反应
C. 原电池的两极一定是活动性不同的两种金属组成
D. 电解时电解池的阳极一定是阴离子放电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2===2NH3的能量变化如图所示,该反应的热化学方程式是( )
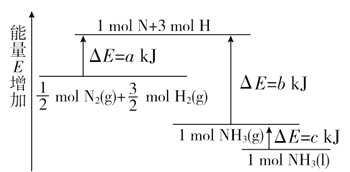
A. N2(g)+3H2(g)===2NH3(l) ΔH=2(a-b-c) kJ·mol-1
B. N2(g)+3H2(g)===2NH3(g) ΔH=2(b-a) kJ·mol-1
C. ![]() N2(g)+
N2(g)+![]() H2(g)===NH3(l) ΔH=(b+c-a) kJ·mol-1
H2(g)===NH3(l) ΔH=(b+c-a) kJ·mol-1
D. ![]() N2(g)+
N2(g)+![]() H2(g)===NH3(g) ΔH=(a+b) kJ·mol-1
H2(g)===NH3(g) ΔH=(a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是( )

A.O2在石墨Ⅱ附近发生氧化反应
B.该电池放电时NO3-向石墨Ⅱ电极迁移
C.石墨Ⅰ附近发生的反应:3NO2 +2e-=NO+ 2NO3-
D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量:
A. 相等 B. 中和HCl的量多
C. 中和CH3COOH的量多 D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体分散系在日常生活中很常见。下列说法正确的是
A.Fe(OH)3易溶于水形成胶体
B.CuSO4溶液可观察到丁达尔现象
C.Fe(OH)3胶体可观察到丁达尔现象
D.胶体分散系中所有粒子的直径都在1~1000 nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO![]() 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是( )
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是( )

A. 反应中转移电子的物质的量是0.21 mol
B. ClO![]() 的生成可能是由于温度升高引起的
的生成可能是由于温度升高引起的
C. 苛性钾溶液中KOH的质量是16.8 g
D. 一定有3.36 L氯气参加反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 某ⅡA族元素的原子序数为a,则原子序数为a+1的元素一定是ⅢA族元素
B. 除短周期外,其他周期均有32种元素
C. 原子最外层只有2个电子的元素可能是金属元素也可能是非金属元素
D. 碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com