
| A、无水醋酸铯的化学式为CH3COOCs,易溶于水,其水溶液显碱性 | B、碳酸氢铯加热即分解生成碳酸铯、二氧化碳和水 | C、在Na、K、Rb、Cs中,Cs熔点最高,密度最大 | D、CsH是离子化合物,与水反应可以生成H2 |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
| 亚硝酸钠(NaNO2) | 氯化钠(NaCl) | |
| 水溶性 | 易溶,溶液呈弱碱性 | 易溶,溶液呈中性 |
| 熔点 | 271℃ | 801℃ |
| 沸点 | 320℃会分解 | 1413℃ |
| 跟稀盐酸作用 | 有红棕色的NO2气体放出 | 无反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
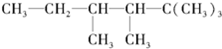
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤不正确 | B、③④⑤不正确 | C、除④外其他都不正确 | D、都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
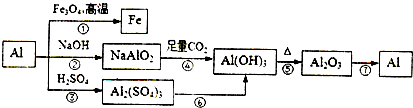
| A、反应①又称铝热反应,可用于野外焊接铁轨 | B、反应②、③都有氢气生成,产生等量的氢气时转移的电子数相等 | C、常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加足量的NaOH溶液 | D、工业上用反应⑦制备铝时,常加入冰晶石以降低氧化铝的熔融温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述I | 叙述II |
| A | NaHCO3能与碱反应 | NaHCO3用作糕点的膨松剂 |
| B | 实验室常用MgSO4溶液与NaOH溶液制备Mg(OH)2沉淀 | Mg(OH)2不溶于强碱 |
| C | Cl2与Fe反应生成FeCl3 | 把FeCl3溶液直接蒸发结晶可以制备出FeCl3固体 |
| D | 铜丝与浓硫酸反应完,冷却后向试管中加入水来观察CuSO4溶液的蓝色 | 铜与浓硫酸反应生成了CuSO4和SO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是
A.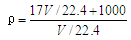 B.
B.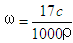
C.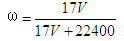 D.
D.
查看答案和解析>>
科目:高中化学 来源:2015届广东省惠州市高三第二次调研考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,2.24L苯中含0.6NA个氢原子
B. 22.4LCl2通入水中充分反应,共转移NA个电子
C. 1L1mol·L-1氯化铜溶液中Cu2+的数目小于NA
D. 0.1mol铁在0.1molCl2中充分燃烧,转移的电子数为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com