
【题目】下列说法正确的是( )
A.其它条件不变时,增大反应物浓度能使活化分子百分数提高,反应速率加快
B.反应物总能量高于生成物总能量的反应,一定能自发进行
C.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同
D.因为催化剂能改变反应活化能,所以能影响化学平衡状态
 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】硼、镁及其化合物在工农业生产中应用广泛.已知:硼镁矿主要成分为![]() ,硼砂的化学式为
,硼砂的化学式为![]() 利用硼镁矿制取金属镁及粗硼的工艺流程如下.
利用硼镁矿制取金属镁及粗硼的工艺流程如下.

回答下列有关问题.
(1)硼砂中B的化合价为 ______,溶于热水后,常用![]() 调pH到
调pH到![]() 制取
制取![]() ,反应的离子方程式为 ______,X为
,反应的离子方程式为 ______,X为![]() 晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为 ______,该反应中的氧化剂是 ______ (填化学式)。
晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为 ______,该反应中的氧化剂是 ______ (填化学式)。
(2)硼酸是一种一元弱酸,它与水作用时结合水电离的![]() 而释放出水电离的H+,这一变化的化学方程式为 ______,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,则硼酸与氢氧化钠反应的离子方程式为 ______。
而释放出水电离的H+,这一变化的化学方程式为 ______,皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,则硼酸与氢氧化钠反应的离子方程式为 ______。
(3)![]() 需要在HCl氛围中加热制
需要在HCl氛围中加热制![]() ,其目的是 ______ .
,其目的是 ______ .
(4)制得的粗硼在一定条件下生成![]() ,
,![]() 加热分解可以得到纯净的单质硼.现将
加热分解可以得到纯净的单质硼.现将![]() 粗硼制成的
粗硼制成的![]() 完全分解,生成的
完全分解,生成的![]() 用
用![]() 为弱酸
为弱酸![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 盛装
盛装![]() 溶液的仪器应为 ______
溶液的仪器应为 ______ ![]() 填“酸式”或“碱式”
填“酸式”或“碱式”![]() 滴定管.该粗硼样品的纯度为 ______ (提示:
滴定管.该粗硼样品的纯度为 ______ (提示:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (x)、
(x)、![]() (y)、
(y)、![]() (z)的分子式均为C5H6。下列说法正确的是
(z)的分子式均为C5H6。下列说法正确的是
A.x、y、z均能使酸性高锰酸钾溶液褪色
B.z的同分异构体只有x和y两种
C.z的一氯代物只有一种,二氯代物只有两种(不考虑立体异构)
D.x分子中所有原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁溶液和过量碳酸氢铵溶液混合,过滤、洗涤、干燥得到碳酸亚铁,在空气中灼烧碳酸亚铁得到铁的氧化物M。利用滴定法测定M的化学式,其步骤如下:
①称取3.92g样品M溶于足量盐酸,并配成100mL溶液A。
②取20.00mL溶液A于锥形瓶中,滴加KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生气泡。
③待气泡消失后,用1.0000 mol·L-1 KI标准溶液滴定锥形瓶中的Fe3+,达到滴定终点时消耗KI标准溶液10.00 mL。
(1)实验中必需的定量仪器有量筒、电子天平、____________和____________。
(2)在滴定之前必须进行的操作包括用标准KI溶液润洗滴定管、__________、___________。
(3)步骤②中“气泡”有多种可能,完成下列猜想:
①提出假设:
假设1:气泡可能是SCN-的反应产物N2、CO2、SO2或N2,CO2。
假设2:气泡可能是H2O2的反应产物____________,理由___________。
②设计实验验证假设1:
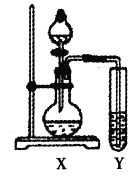
试管Y中的试剂是_______。
(4)根据上述实验,写出硫酸亚铁溶液和过量碳酸氢铵溶液混合制备碳酸亚铁的离子方程式_____。
(5)根据数据计算,M的化学式为_______。
(6)根据上述实验结果,写出碳酸亚铁在空气中灼烧的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.放热反应一定能自发的进行
B.SO2能使品红溶液和溴水褪色,说明SO2具有漂白性
C.将AlCl3溶液和Al2(SO4) 3溶液分别蒸干灼烧,所得产物均为Al2O3
D.由反应AgCl(s) +KI(aq)![]() Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I)
Ag I(s) + KCl (aq) 可知Ksp(AgCl)>Ksp(Ag I)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为142.9kJg-1,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l) △H=-285.8kJmol-1
B.反应A(g)=2B(g),若正反应的活化能为EakJmol-1,逆反应的活化能为EbkJmol-1,则△H=(Ea-Eb)kJmol-1
C.能自发进行的化学反应,一定是△H<0、△S>0
D.增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuSO4溶液。
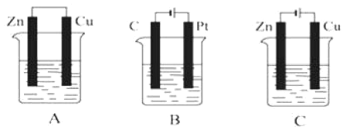
(1)A、B、C三个装置中属于原电池的是___(填字母,下同),属于电解池的是___。
(2)A池中Cu电极上发生的是___(填“氧化”或“还原”)反应。
(3)B池中C是___极,Pt极发生的反应的电极反应式为___。
(4)C池反应过程中,CuSO4溶液的物质的量浓度___(填“变大”“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列设计方案都正确的是( )
A.制备绿矾(FeSO47H2O):将FeSO4溶液在空气中低温蒸发即得绿矾
B.将0.1000mol/L的KMnO4溶液装在碱式滴定管中滴定未知浓度的过氧化氢溶液,读出消耗的高锰酸钾的体积即可求出过氧化氢的浓度
C.探究催化剂对H2O2分解速率影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象
D.用一定浓度的盐酸标准液滴定未知浓度的氨水,可选用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在室温下可能大量共存的是( )
A.pH=2的溶液:HCO3-、Na+、ClO-、NO3-
B.![]() =106的溶液:Al3+、NH4+、CO32-、S2-
=106的溶液:Al3+、NH4+、CO32-、S2-
C.水电离出的c(H+)=10-4mol/L的溶液:Na+、Fe3+、SO42-、Cl-
D.使石蕊呈红色的溶液:NH4+、NO3-、AlO2-、I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com