
| 选项 | 含氧化合物 |
| A | K2O2 |
| B | H2O2 |
| C | Na2CO3 |
| D | Na2O2 |
| A. | A | B. | B | C. | C | D. | D |
分析 钠离子、钾离子的化合价都是+1价,双氧水中氢元素为+1价,然后根据化合物中总化合价为0计算出氧元素的化合价即可.
解答 解:A.K2O2中钾离子的化合价为+1价,则两个O原子的化合价为-2,所以氧元素的化合价为-1价;
B.H2O2中氢元素的化合价为+1价,则两个O原子的总化合价为-2,所以氧元素的化合价为-1价;
C.碳酸钠中碳酸根离子带有2个负电荷,氧元素的化合价为-2价;
D.Na2O2中钠与水的化合价为+1价,则两个O原子的总化合价为-2,所以氧元素的化合价为-1价;
根据分析可知,氧元素的化合价最低的为碳酸钠,
故选C.
点评 本题考查了化合物中化合价计算与判断,题目难度不大,明确常见元素的化合价为解答关键,注意化合物中各元素的总化合价之和为0,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 铜丝与硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 少量碳酸氢钠与氢氧化钙反应:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| C. | 稀盐酸与氢氧化钠溶液混合:H++OH-═H2O | |
| D. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砒霜不是碱性氧化物 | B. | Na3As04是可熔性的正盐 | ||
| C. | 砒霜有剧毒,具有还原性 | D. | AsH3是氢化物,稳定性较强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(HF)<c(F-) | B. | c(Na+)<c(F-) | ||
| C. | c(F-)-c(HF)=c(H+)-c(OH-) | D. | c(HF)+c(F-)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH<7的溶液中:Al3+、K+、SO32-、Cl- | |
| B. | 加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、NO3- | |
| C. | 能使pH试纸变深蓝色的溶液中:S2-、SO32-、S2O32-、SO42- | |
| D. | 由水电离出的[OH-]=1×10-13mol/L的溶液中:Fe2+、NH4+、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
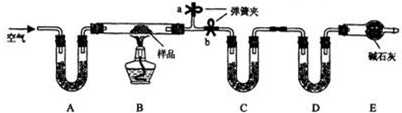
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O2和Na2O | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com