
(10分)A、B、C、 D、 E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①将1L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为:y<x;
②浓度均为0.1mol·L-1A和E溶液,pH:A<E;
③浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。回答下列问题:
(1)E是 溶液。
(2) 用水稀释0.1 mol·L-1B时,溶液中随着水量的增加而减小的是 (填写序号) 。
① ②
② ③c(H+)
③c(H+)
④ OH-的物质的量 ⑤ c(H+)和c(OH-)的乘积
(3)OH-浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,下列说法正确的是 (填写序号) 。
①反应所需要的时间E>A ②开始反应时的速率A>E
③参加反应的锌粉物质的量A=E ④反应过程的平均速率 E>A
⑤A溶液里有锌粉剩余 ⑥E溶液里有锌粉剩余
(4)室温下,将pH=1的A溶液aL与pH=12的 D溶液bL混合,所得混合液的pH=3,设混合溶液体积变化忽略不计,则a:b= 。
(5)0.1 mol·L-1C溶液中各种离子浓度由大到小的顺序是:
。
(1)CH3COOH(2分)
(2)①②(2分)
(3)③④⑤(2分)
(4)1:9(2分)
(5) c(H+)>c (SO42-)> c(NH4+)>c(OH-)(2分)
【解析】
试题分析:
(1)中和酸性物质A只有NaOH、NH3•H2O,物质的量的A与等物质的量浓度B和D混合呈中性,D的用量少,说明D碱性比B的碱性强,所以D是NaOH,由于A的PH小于E,则A为盐酸,则E为醋酸,而C与D中和后显酸性,则C为NH4HSO4;
(2)①、由NH3•H2O⇌OH-+NH4+可知,加水促进电离,则n(NH3•H2O)减少,n(OH-)增大,则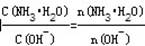 减小,故①错误;②、由NH3•H2O⇌OH-+NH4+可知,加水促进电离,则n(NH3•H2O)减少,n(OH-)增大,c(NH3•H2O)、c(OH-)都减小,c(H+)减小,则
减小,故①错误;②、由NH3•H2O⇌OH-+NH4+可知,加水促进电离,则n(NH3•H2O)减少,n(OH-)增大,c(NH3•H2O)、c(OH-)都减小,c(H+)减小,则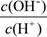
减小,故②正确;③、因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,故③错误;④、由NH3•H2O⇌OH-+NH4+可知,加水促进电离,OH-的物质的量增大,故④错误;所以答案为:①②;
(3)①根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,产生的氢气一样多,反应所需要的时间HCl>CH3COOH,故①错误;②根据酸能与锌反应得到氢气,开始溶液中c(H+)相等,反应时的速率HCl=CH3COOH,故②错误;③根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故③正确;④根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,故④正确;⑤根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑤正确;⑥根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑥错误;所以答案为:③④⑤;
(4)根据PH计算:(0.1a-0.1b)/(a+b)=0.001,设a=1,则b=9
(5)由于水也电离出了氢离子,所以氢离子的量大于硫酸根离子,而铵根离子会发生水解,所以铵根离子的量小于硫酸根离子,最少的是氢氧根离子。
考点:弱电解质在水溶液中的电离平衡;离子浓度大小的比较
点评:考查电解质溶液之间的反应,涉及到强电解质、弱电解质的电离、盐类的水解及溶液的pH值、离子浓度大小的比较等知识。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含1~18号元素中的某 一 元素,它们按图所示关系相互转化,已知A为单质.查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:

| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(F)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com