
(2分)某气体的分解反应在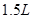 的容器中进行,8分钟消耗反应物
的容器中进行,8分钟消耗反应物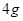 。在另一条件下,该气体在
。在另一条件下,该气体在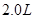 容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为
。
容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为
。
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验 | 外加试剂 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸 | 迅速变棕褐色 |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
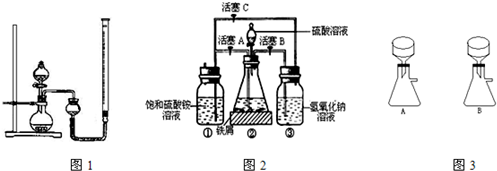
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果。某兴趣小组通过实验研究MnO2的性质![]()
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 。
A、把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B、把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C、把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D、把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验。
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
该小组从上述对比实验中,可以得出的结论是 。
写出在酸性条件下,MnO2氧化I-的离子方程式 。
(3)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1g/cm3)配制浓度3%的H2O2溶液(密度近似为1g/cm3)100mL。其配制方法是:用量筒量取 mL30%H2O2溶液放入 (填仪器名称)中,再加入一定量的水,搅拌均匀。
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡。该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用。请设计一个简单实验证明该假设是否正确。
。
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是 (填序号)。
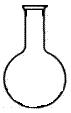
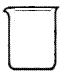

![]()
A B C D
(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省武威第五中学高二9月月考化学试卷(带解析) 题型:填空题
(2分)某气体的分解反应在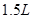 的容器中进行,8分钟消耗反应物
的容器中进行,8分钟消耗反应物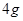 。在另一条件下,该气体在
。在另一条件下,该气体在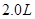 容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为 。
容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com