
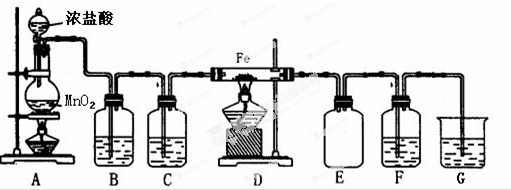
分析 (1)实验室用浓盐酸与二氧化锰加热制备氯气,用分液漏斗盛放滴加浓盐酸;
(2)由于盐酸易挥发,制备的氯气中含有HCl和水蒸气,饱和食盐水吸收HCl,用浓硫酸干燥氯气;
(3)氯气与铁反应生成氯化铁;
(4)氯气溶液水与水反应生成氯化氢和次氯酸,氯化氢电离生成氯离子和氢离子,氯离子能够与硝酸银电离出的银离子反应生成白色氯化银沉淀;
(5)氯气有毒能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,可以用氢氧化钠吸收过量的氯气.
解答 解:(1)实验室用浓盐酸与二氧化锰加热制备氯气,方程式:4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O,用分液漏斗盛放滴加浓盐酸;
故答案为:分液漏斗;4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O;
(2)由于盐酸易挥发,制备的氯气中含有HCl和水蒸气,饱和食盐水吸收HCl,用浓硫酸干燥氯气;
故答案为:饱和食盐水;干燥(除去水蒸气);
(3)氯气与铁反应生成氯化铁,反应的方程式:3C12+2Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
故答案为:3C12+2Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(4)氯气溶液水与水反应生成氯化氢和次氯酸,氯化氢电离生成氯离子和氢离子,氯离子能够与硝酸银电离出的银离子反应生成白色氯化银沉淀;,所以看到现象为:有白色沉淀生成;
故答案为:有白色沉淀生成;HCl;
(5)氯气有毒能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,化学方程式:2NaOH+Cl2=NaCl+NaClO+H2O,可以用盛有氢氧化钠的装置G吸收过量的氯气;
故答案为:除去多余的氯气,防止污染空气;2NaOH+Cl2=NaCl+NaClO+H2O.
点评 本题考查氯气实验制备与氯气的性质实验,涉及对装置的分析与评价,熟悉氯气制备原理和性质即可解答,题目难度不大.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | 氯化铁溶液滴加到沸水中得到Fe(OH)3 胶体:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| C. | 铁溶于盐酸产生H2:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaNO2是还原剂 | |
| B. | NH4Cl中N元素被还原 | |
| C. | 生成1 mol N2时转移6 mol电子 | |
| D. | 氧化剂和还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(NO3)2和KOH | B. | Ca(ClO)2和Na2CO3 | C. | (NH4)2SO4和BaCl2 | D. | K2SO4和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64 g•mol-1 | B. | 24 g•mol-1 | C. | 56 g•mol-1 | D. | 188 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2(s)与CO2(g)反应时,放出226kJ热量 | |
| B. | CO的燃烧热为△H=-566kJ/mol | |
| C. | CO(g)与Na2O2 (S)反应的热化学方程式为:Na2O2(s)+CO(g)═Na2CO3(s)△H=-509kJ•mol-1 | |
| D. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g)△H=-452kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L KNO3溶液:、H+、Fe2+、Al3+、Cl- | |
| B. | 酸性溶液:NH4+、Fe2+、K+、SO42- | |
| C. | 碱性溶液:ClO-、SO32-、K+、Na+ | |
| D. | 与铝反应产生大量氢气的溶液:K+、Cl-、CO32-、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com