
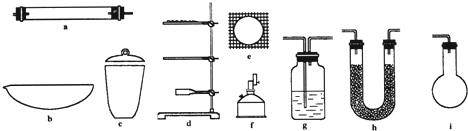
分析 (1)测定有机物的实验式,就要测定有机物本身的质量、CO2和水的质量,测定水的质量可用无水氯化钙吸收,测定CO2的质量可用KOH浓溶液吸收,分别称取吸收前后的吸收剂的质量,计算碳、氢原子在分子中的含量,装置h即可盛无水氯化钙也可盛KOH浓溶液;
(2)如果试样质量=碳元素质量+氢元素质量为烃,如果试样质量>碳元素质量+氢元素质量为烃的含氧衍生物;
(3)求得了实验式,要求得分子式,必须知道该有机物的相对分子质量.
解答 解:(1)测定有机物的实验式,就要测定有机物本身的质量、CO2和水的质量,测定水的质量可用无水氯化钙吸收,测定CO2的质量可用KOH浓溶液吸收,分别称取吸收前后的吸收剂的质量,计算碳、氢原子在分子中的含量,装置h即可盛无水氯化钙也可盛KOH浓溶液,因此最少需要的仪器种类为4种,分别是a、d、f、h,两次用到h,前者盛有无水氯化钙吸收水,后者盛有KOH浓溶液吸收CO2,需要用天平称量质量,
故答案为:4;a、d、f、h;h;吸收H2O;吸收CO2;天平;
(2)根据质量守恒定律,如果试样质量=碳元素质量+氢元素质量为烃,如果试样质量>碳元素质量+氢元素质量为烃的含氧衍生物,
故答案为:试样质量=碳元素质量+氢元素质量为烃,试样质量>碳元素质量+氢元素质量为烃的含氧衍生物;
(3)定温、定压下蒸气密度之比等于相对分子质量之比,求得了实验式和相对分子质量即可得到该有机物的化学式,
故答案为:B.
点评 本题考查有机物实验式和分子式的确定,难度不大,了解希比希元素分析法的原理和方法是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol/(L•s) | B. | v(B)=0.005 mol/(L•s) | ||
| C. | v(C)=0.8 mol/(L•min) | D. | v(D)=1.0 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2SO3制备少量SO2:SO${\;}_{3}^{2-}$+2H+═SO2↑+H2O | |
| B. | Na2SO3溶液使酚酞试剂变红:SO${\;}_{3}^{2-}$+H2O═OH-+HSO${\;}_{3}^{-}$ | |
| C. | 用Ba(NO3)2溶液检验HSO${\;}_{3}^{-}$:HSO${\;}_{3}^{-}$+Ba2+═BaSO3↓+H+ | |
| D. | 用NaHSO3溶液检验H2S气体:2H2S+H++HSO${\;}_{3}^{-}$═3S↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式分别为C2H6和C4H10的两种有机化合物一定互为同系物 | |
| B. | 某反应过程中的能量变化如图所示,可见催化剂能改变该反应的焓变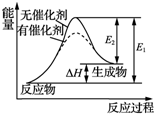 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 1 mol N2与3 mol H2在一定条件下充分反应可得2 mol NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com