
���� ��1��������ȫ��Ӧ��������Ϊ1g������n=$\frac{m}{M}$�������ʵ���֮�ȣ����ݵ���ת���غ���������������ʵ�������ͬ�����£��������֮�ȵ��������ʵ���֮�ȣ�
��2��������ȫ��Ӧ������������ʵ���Ϊ1mol�����ݵ���ת���غ�����������������ʵ���֮�ȣ�����m=nM��֪��������֮�ȵ��������ʵ���֮�ȣ�
��3����ͬ�������������������ȣ������������ʵ�����ȣ������������ʵ���Ϊ1mol�����ݵ���ת���غ������������ʵ������ٽ��m=nM��������֮�ȣ�
��� �⣺��1��������ȫ��Ӧ��������Ϊ1g����Na��Mg��Al�����ʵ���֮��Ϊ$\frac{1}{23}$��$\frac{1}{24}$��$\frac{1}{27}$�����ݵ���ת���غ㣬�����������ʵ���֮��Ϊ$\frac{1}{23}$��1��$\frac{1}{24}$��2��$\frac{1}{27}$��3=$\frac{1}{23}$��$\frac{1}{12}$��$\frac{1}{9}$������ͬ�����������������֮��Ϊ��$\frac{1}{23}$��$\frac{1}{12}$��$\frac{1}{9}$��
�ʴ�Ϊ��$\frac{1}{23}$��$\frac{1}{12}$��$\frac{1}{9}$��
��2��������ȫ��Ӧ������������ʵ���Ϊ1mol�����ݵ���ת���غ㣬�������������ʵ���֮��Ϊ1mol��1��1mol��2��1mol��3=1��2��3����������������֮��Ϊ1��2��3��
�ʴ�Ϊ��1��2��3��
��3����ͬ�������������������ȣ������������ʵ�����ȣ������������ʵ���Ϊ1mol�����ݵ���ת���غ㣬��ҪNa�����ʵ���=$\frac{1mol��2}{1}$=2mol��Mg�����ʵ���=$\frac{1mol��2}{2}$=1mol��Al�����ʵ���=$\frac{1mol��2}{3}$=$\frac{2}{3}$mol������ҪNa��Mg��Al�����ʵ���֮��=2mol��1mol��$\frac{2}{3}$mol=6��3��2��Na��Mg��Al������֮��=2mol��23g/mol��1mol��24g/mol��$\frac{2}{3}$mol��27g/mol=23��12��9��
�ʴ�Ϊ��23��12��9��6��3��2��
���� ���⿼�����ʵ����йؼ��㡢��ѧ����ʽ���㣬�Ƚϻ�����ע�����õ���ת���غ���㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
| ��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
| ��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ܶ� | B�� | �����������ѹǿ | ||
| C�� | ��������ƽ����Է������� | D�� | A��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
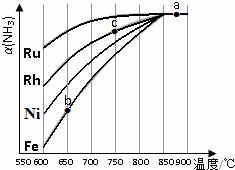 ����������������Ϳ�����Ӧ��ʮ�ֹ㷺
����������������Ϳ�����Ӧ��ʮ�ֹ㷺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��ѧ�ĺ�����Ӧ�û�ѧԭ���Ի�����Ⱦ�������� | |
| B�� | PM2.5��������������������ж��к����ʣ����˵ķι�����ɺܴ�Σ�� | |
| C�� | ��������㷺Ӧ����̫���ܵ�ء������оƬ | |
| D�� | ����β���к��д���������Ⱦ��������Ͳ���ȫȼ����ɵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��M���ף���M���ң�������������ף��� | B�� | ��M���ף���M���ң���������Ħ��������ף��� | ||
| C�� | ��M���ף���M���ң����������ѹǿ���ף��� | D�� | ��M���ף���M���ң���������������ף��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgO���壨SiO2�����ӹ���NaOH��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ����� | |
| B�� | CO2��SO2��������KMnO4��Һ��Ũ���ᣬϴ�� | |
| C�� | KNO3���壨NaCl��������ˮ�ܽ⡢�������ᾧ�����ˡ�ϴ�ӡ����� | |
| D�� | FeCl3��Һ��CuCl2�����������ۣ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ����ʹ�����������ɫ��ȥ��˵��Ũ���������ˮ�� | |
| B�� | ����ֲ������ĸ��������Խ������еĵ�������̬תΪ����̬�ǵ��Ĺ̶� | |
| C�� | �����£�Ũ����������������棬˵������Ũ�����Ӧ | |
| D�� | ��ˮ��ʹ��̪�Լ���Ϊ��ɫ��˵����ˮ�Լ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
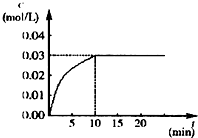 ��ijһ�ݻ�Ϊ5L���ܱ������ڣ����� 0.2mol��CO��0.2mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g������H��0����Ӧ��CO2��Ũ����ʱ��仯�����ͼ��
��ijһ�ݻ�Ϊ5L���ܱ������ڣ����� 0.2mol��CO��0.2mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g������H��0����Ӧ��CO2��Ũ����ʱ��仯�����ͼ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com