
【题目】对于100mL1mol/L硫酸与铁片的反应,采取下列措施,其中能使反应速率加快的是
A. 再加入等量的铁片 B. 改用200mL 1.5mol/L盐酸
C. 改用浓硫酸 D. 升高温度
【答案】D
【解析】A项,再加入等量的铁片,化学反应速率不变;B项,改用200mL1.5mol/L盐酸,c(H+)减小,化学反应速率减慢;C项,Fe与浓硫酸常温下发生钝化;D项,升高温度化学反应速率加快。
A项,铁片为固体,再加入等量的铁片,化学反应速率不变;B项,Fe与稀硫酸的反应为Fe+2H+=Fe2++H2↑,1mol/LH2SO4溶液中c(H+)=2mol/L,改用200mL1.5mol/L盐酸,1.5mol/L盐酸中c(H+)=1.5mol/L![]() 2mol/L,c(H+)减小,化学反应速率减慢;C项,Fe与浓硫酸常温下发生钝化;D项,升高温度化学反应速率加快;能使化学反应速率加快的是升高温度,答案选D。
2mol/L,c(H+)减小,化学反应速率减慢;C项,Fe与浓硫酸常温下发生钝化;D项,升高温度化学反应速率加快;能使化学反应速率加快的是升高温度,答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
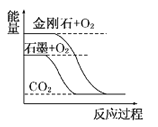

据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应 B. 白磷比红磷稳定
C. S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2 D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于酶的叙述中正确的是 ( )
A.由有分泌功能的细胞产生,并且能调节生物体的生命活动
B.生物体内的酶在不断更新
C.都是在核糖体上合成的
D.与双缩脲试剂发生作用都可产生紫色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】推理是化学学习中常用的思维方法,下列推理合理的是
A. NaOH和CaCl2都是离子化合物,所以二者化学键类型相同
B. 可逆反应达平衡时,体系中各组分的浓度不再变化,可推知正、逆反应停止了
C. 原电池加快某些反应的速率,所以用锌与稀硫酸反应制取氢气常加入少量硫酸铜
D. 同条件下反应物浓度越大反应越快,所以铁在浓硝酸中比在稀硝酸中溶解得快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E的产量是衡量一个国家石油化工水平发展的标志,F为高分子化合物,能进行如图所示的反应. 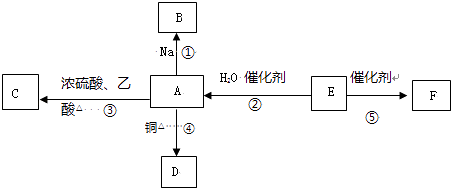
(1)请写出E的电子式 .
(2)下列反应的化学方程式:(要求有机物必须写结构简式) 反应②: 反应类型 .
反应④:反应类型 .
反应⑤:反应类型 .
(3)比较反应①剧烈程度(填>、=或<)钠和水反应的烈程度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中M的分解速率的影响因素进行研究。 在相同温度下,M的物质的量浓度[c(M)]随时间(t)的变化如下图所示。下列说法错误的是

A. 水样酸性越强,M的分解速率越快
B. 水样中添加Cu2+,能加快M的分解速率
C. 由②③得,反应物浓度越大,M的分解速率越快
D. 在0~20 min内,②中M的分解速率为0.015 mol·L1·min1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·Lˉ1 NaOH溶液至铜离子恰好完全沉淀,则消耗NaOH溶液的体积是
A. 15mL B. 30mL C. 45mL D. 60mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的信息,下列叙述正确的是( )

A. 2 mol H2(g)跟 1 mol O2(g)反应生成 2 mol H2O(g)吸收能量为490kJ
B. 化学反应中能量变化的大小与反应物的质量多少无关
C. 1 mol H2(g) 跟0.5mol O2(g) 反应生成 1 mol H2O(l)释放能量为2465kJ
D. 2molH2O (g)的能量比2 mol H2(g)与1 mol O2(g)的能量之和低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中属于强电解质且能导电的是( )
①氢氧化钠溶液 ②硫酸钙固体 ③铜 ④蔗糖 ⑤三氧化硫 ⑥熔融氯化钠
A.①②⑤B.⑥C.③⑥D.①②⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com