
����Ŀ��(1)ά����A�������ر��Ƕ��˵���������Ҫ���ã���ṹ��ʽ���£�

1 mol�û��������________mol Br2�����ӳɷ�Ӧ��
(2)���л���Ӧ�У���Ӧ����ͬ��������ͬ���ɵõ���ͬ���������ʽ��R���������������������ȥ��

(��ע��H��Br�ӳɵ�λ��)
��д��ʵ������ת��ĸ�����Ӧ�Ļ�ѧ����ʽ���ر�ע��д����Ӧ������
����CH3CH2CH2CH2Br������ת��ΪCH3CH2CHBrCH3��__________________��___________________��
����(CH3)2CHCH===CH2������ת��Ϊ(CH3)2CHCH2CH2OH��__________________��____________________��
���𰸡� 5 CH3CH2CH2CH2Br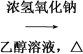 CH3CH2CH===CH2��HBr�� CH3CH2CH===CH2
CH3CH2CH===CH2��HBr�� CH3CH2CH===CH2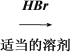 CH3CH2CHBr��CH3 (CH3)2CHCH===CH2
CH3CH2CHBr��CH3 (CH3)2CHCH===CH2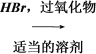 (CH3)2CHCH2CH2Br (CH3)2CHCH2CH2Br��H2O
(CH3)2CHCH2CH2Br (CH3)2CHCH2CH2Br��H2O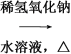 (CH3)2CHCH2CH2OH��HBr
(CH3)2CHCH2CH2OH��HBr
����������1��ά����A�к���5��̼̼˫����1 mol�û��������5mol Br2�����ӳɷ�Ӧ����2������CH3CH2CH2CH2Br������ת��ΪCH3CH2CHBrCH3�������Ϣ��֪��Ӧ�ȷ�����ȥ��Ӧ����1-��ϩ��Ȼ����HBr�����ӳɷ�Ӧ�������ķ�ӦΪCH3CH2CH2CH2Br![]() CH3CH2CH=CH2��CH3CH2CH=CH2HBr
CH3CH2CH=CH2��CH3CH2CH=CH2HBr![]() CH3CH2CHBrCH3�����ɣ�CH3��2CHCH=CH2������ת��Ϊ��CH3��2CHCH2CH2OH��-OH�ڶ�̼ԭ���ϣ�����HBr�ڹ����������������ɣ�CH3��2CHCH2CH2Br�����ڼ�����Һ��ˮ�⣬�����ķ�ӦΪ��CH3��2CHCH=CH2��HBr
CH3CH2CHBrCH3�����ɣ�CH3��2CHCH=CH2������ת��Ϊ��CH3��2CHCH2CH2OH��-OH�ڶ�̼ԭ���ϣ�����HBr�ڹ����������������ɣ�CH3��2CHCH2CH2Br�����ڼ�����Һ��ˮ�⣬�����ķ�ӦΪ��CH3��2CHCH=CH2��HBr![]() ��CH3��2CHCH2CH2Br����CH3��2CHCH2CH2Br
��CH3��2CHCH2CH2Br����CH3��2CHCH2CH2Br![]() ��CH3��2CHCH2CH2OH��
��CH3��2CHCH2CH2OH��


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪ��Ӧ2H2��g��+O2��g���T2H2O��g���������仯ʾ��ͼ������˵����ȷ����

A��H2��g����O2��g����Ӧ����H2O��g�������Ǹ����ȷ�Ӧ����
B����2mol H2��1mol O2���4mol H��2mol Oԭ�ӣ����Ǹ����ȷ�Ӧ����
C��2mol H2��g����1mol O2��g����Ӧ����2mol H2O��g�������ų�484kJ����
D��4mol H��2mol O����2mol H2O��g�������ų�484kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �õ���Խ�࣬��������Խǿ
B. ������ֻ�������ԣ�������ֻ�л�ԭ��
C. Ҫ���SO32-��SO42-��ת�����������������
D. ��ʹʯ����Һ��������Һ�д����������ӣ�Na+��K+��NO3-��Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ü�������������ȡ����Ӧ��ȡ����Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС����ʵ������ģ���������̡�����Ƶ�ģ��װ�����£�

����Ҫ����գ�
(1)Bװ�������ֹ��ܣ������Ȼ�����壻�� ���� ��
(2)��V(Cl2)/V(CH4)��x��������������������Ȼ��⣬��xֵӦ ��
(3)Dװ�õ�ʯ���о��Ȼ���KI��ĩ���������� ��
(4)Eװ�õ������� (����)��
A���ռ����� B.��������
C����ֹ���� D�������Ȼ���
(5)Eװ�ó����������⣬�������л����E�з�����������ѷ���Ϊ (����뷽������)��
(6)��װ�û���ȱ�ݣ�ԭ����û�н���β����������β����Ҫ�ɷ�Ϊ (����)��
A.CH4B��CH3C1 C��CH2C12D��CHCl3E��CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4��Ӧ�У���������Pԭ���뱻��ԭ��Pԭ�Ӹ�������
A. 6:5 B. 5:6 C. 11:5 D. 11:6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������ݣ�
���� | �۵�(��) | �е�(��) | �ܶ�(g��cm��3) |
�Ҵ� | ��117.0 | 78.0 | 0.79 |
���� | 16.6 | 117.9 | 1.05 |
�������� | ��83.6 | 77.5 | 0.90 |
ijѧ����ʵ������ȡ������������Ҫ�������£�

������2 mLŨ���ᡢ3 mL�Ҵ�(��18O)��2 mL����Ļ����Һ��
������ͼ���Ӻ�װ��(װ������������)��������Һ����С����ȼ���3 min��5 min��
�����Թ����ռ���һ���������ֹͣ���ȣ������Թ��Ҳ�������Ȼ���ô��ֲ㡣
�����������������ϴ�ӡ����
(1)��Ӧ��Ũ�����������______________________________________��
д����ȡ���������Ļ�ѧ����ʽ��_____________________________��
(2)����ʵ���б���̼������Һ��������________(����ĸ)��
A���к�������Ҵ� B���к����Ტ�����Ҵ�
C�����������������ܽ� D�������������ɣ���������
(3)����������ҪС����ȼ��ȣ�����Ҫ������___________________��
���������۲쵽��������_____________________________________��
�������Թ��е����ʷ����Եõ���������������ʹ�õ�������________������ʱ����������Ӧ������________(�����¿ڷ��������Ͽڵ���)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н����У�������Ȼ�γɵ��������ܱ����ڲ��������������������
A. Al B. Na C��Fe D. K
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯���漰������ԭ��Ӧ���ǣ� ��
A.������ˮ
B.��������
C.��ˮ����
D.��ҵ�̵�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ����������Һ�������ڣ����������۾����������
B. �·�մ�ϴ�����Ũ����������Һ���轫���·�������ʢˮ������
C. Ƥ���Ͻ��н϶��Ũ���ᣬֱ����ˮ��ϴ����
D. ʵ�����ϵľƾ����㵹��ȼ��������������ʪ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com