
| 8 |
| 3 |
| 2 |
| 3 |
| 4 |
| 3 |
| 8 |
| 3 |


科目:高中化学 来源: 题型:阅读理解
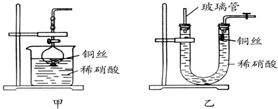 NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.| 浓硝酸 |
| 稀硝酸 |
| 氯气 |
| 硝酸 |
| 空气 |
| 硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列物质制取相同质量的Cu(NO3)2,消耗硝酸的量最多的是( )
A.CuO+浓HNO3 B.Cu+稀HNO3 C.Cu+浓HNO3 D.Cu(OH)2+HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
要制取相同质量的Cu(NO3)2,下列反应中消耗HNO3最少的反应是( )
A.Cu和浓HNO3 B. Cu和稀HNO3
C. CuO和HNO3 D.Cu2O和HNO3
查看答案和解析>>
科目:高中化学 来源:2014届福建省四地六校高一下学期第二次联考化学试卷(解析版) 题型:选择题
要制取相同质量的Cu(NO3)2,下列反应中消耗HNO3最少的反应是( )
A.Cu和浓HNO3 B. Cu和稀HNO3
C. CuO和HNO3 D.Cu2O 和HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com