
| A、将氨水逐滴滴入AgNO3溶液中,至过量 |
| B、将二氧化碳通入Ca(OH)2 溶液中,至过量 |
| C、将氯气通入AgNO3溶液中好,至过量 |
| D、将二氧化氮通入Ba(OH)2 溶液中,至过量 |


科目:高中化学 来源: 题型:
| A、用加热蒸发Na2CO3溶液的方法除去少量NaHCO3 |
| B、向含有少量Fe3+的CuSO4溶液中加入铜片除去Fe3+ |
| C、用加热的方法分离NH4Cl和碘固体混合物 |
| D、用二氧化锰区别10%的H2O2溶液和10%的稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、2:3 |
| C、2:7 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
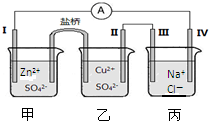 某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )
某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )| A、电子由电极Ⅳ通过外电路流向电极Ⅰ |
| B、装置工作过程中Ⅲ电极周围出现红色 |
| C、电极Ⅱ发生还原反应 |
| D、盐桥中Cl-向乙池移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
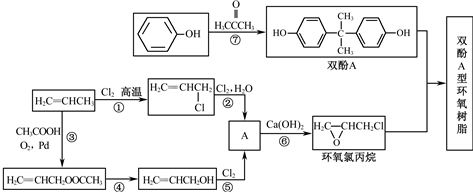
 )合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户).写出此合成反应的化学方程式:
)合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户).写出此合成反应的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com