(2011?德州一模)在实验室中用下列装置进行有关实验探究.请回答下列问题:
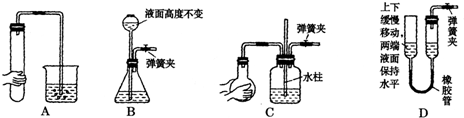
Ⅰ.气体制备时需检查装置的气密性,如下图所示各装置,肯定不符合气密性检查要求的是
D
D
.
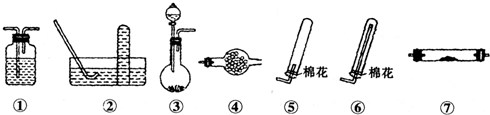
Ⅱ.若用下列装置③制取并收集干燥的NH
3,烧瓶内装的试剂是
生石灰
生石灰
.收集装置应选择
⑥
⑥
(填装置序号).证明氨气已收集满的操作是
将湿润的红色石蕊试纸靠近瓶口,试纸变蓝(或将蘸有浓盐酸的玻璃棒靠近瓶口,有白烟生成)
将湿润的红色石蕊试纸靠近瓶口,试纸变蓝(或将蘸有浓盐酸的玻璃棒靠近瓶口,有白烟生成)
.
Ⅲ.二氯化二硫(S
2Cl
2)在工业上用于橡胶的硫化.为在实验室合成S
2Cl
2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S
2Cl
2粗品.
②有关物质的部分性质如下表:
| 物质 |
熔点/℃ |
沸点℃ |
化学性质 |
| S |
112.8 |
444.6 |
略 |
| S2Cl2 |
-77 |
137 |
遇水生成HCl,SO2,S;300℃以上完全分解;
S2Cl2+Cl22SCl2 |
设计实验装置图如下:
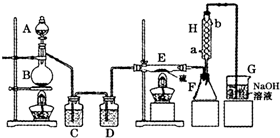
(1)B中反应的离子方程式:
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
;
(2)H中冷水的方向为
a
a
进
b
b
出.
(3)为了提高S
2Cl
2的纯度,关键的操作是控制好温度和
控制浓盐酸的滴速不要过快
控制浓盐酸的滴速不要过快
.
(4)尾气处理装置存在明显的缺陷,如何改正:
在G和H之间增加干燥装置;G中加防倒吸装置
在G和H之间增加干燥装置;G中加防倒吸装置
.






 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案


