
【题目】下列有关说法不正确的是( )
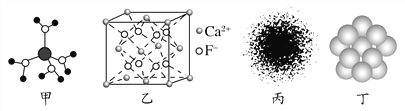
A. 水合铜离子的模型如图甲所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图乙所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图丙所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图丁所示,为最密堆积,每个Cu原子的配位数均为12
科目:高中化学 来源: 题型:
【题目】近年来新闻媒体不断报道有人误将亚硝酸钠(NaNO2)当食盐用,发生中毒事件甚至造成死亡。亚硝酸钠中N为+3价,处于中间价态,既有氧化性又有还原性,在酸性环境中可以还原高锰酸钾,使KMnO4溶液的紫色褪去。在酸性环境中还可以将I-氧化成I2 , I2能使淀粉变蓝。为了区别食盐和亚硝酸钠,老师提供了下表中的试剂、操作供学生选择。
试剂 | 操作 |
①H2SO4溶液 | a.把样品放入H2SO4溶液中,再加入淀粉溶液 |
②KMnO4溶液 | b.把样品放入H2SO4溶液中,溶解后再加入所选试剂 |
③KI溶液 | c.把样品放入水中,溶解后再加入所选试剂 |
④AgNO3溶液 | d.把样品放入盐酸中再加入所选试剂 |
⑤淀粉溶液 |
(1)能判断被检验的样品是食盐的试剂和操作是 , 现象及结论是。
(2)请用两套方案判断被检验的样品是亚硝酸钠。 方案一:试剂及操作: , 现象:。
方案二:试剂及操作: , 现象:。
(3)某同学检验样品是亚硝酸钠时采用了②、D的组合,是否可行? , 原因是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应经常伴随着颜色变化,下列有关反应的颜色变化描述正确的是( )
①二氧化硫通入品红溶液→无色
②淀粉溶液遇单质碘→蓝色
③溴化银见光分解→白色
④热的氧化铜遇乙醇→绿色
A.①②③B.②④C.①②D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应原理中,不符合工业冶炼金属实际情况的是( )
A.2Ag2O ![]() 4Ag+O2↑
4Ag+O2↑
B.2Al2O3(熔融) ![]() 4Al+3O2↑
4Al+3O2↑
C.2MgO ![]() 2Mg+O2↑
2Mg+O2↑
D.4CO+Fe3O4 ![]() ?3Fe+4CO2
?3Fe+4CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在生产生活中应用十分广泛。请回答下列问题:
(1)通过SO2传感器可监测大气中SO2的含量,其工作原理如图所示。
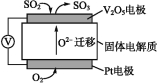
①固体电解质中O2向 (填“正”或“负”)极移动。
②写出V2O5电极的电极反应式: 。
(2)如图所示装置(Ⅰ)是一种可充电电池,装置(Ⅱ)是一种以石墨为电极的家用环保型消毒液发生器。装置(Ⅰ)中离子交换膜只允许Na+通过,充、放电的化学方程式为2Na2S2+NaBr3![]() Na2S4+3NaBr。
Na2S4+3NaBr。
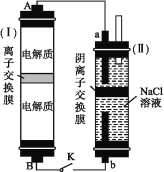
①负极区的电解质为 (用化学式表示)。
②家用环保型消毒液发生器发生反应的离子方程式为 。
③闭合开关K,当有0.04 mol Na+通过离子交换膜时,a电极上析出的气体在标准状况下的体积为
mL。
(3)下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“![]() +2I+2H+
+2I+2H+![]()
![]() +I2+H2O”设计成的原电池装置,其中C1、C2、C3、C4均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸或40% NaOH溶液,电流表指针都不发生偏转;乙组经思考后先添加了一种离子交换膜,然后向图Ⅱ烧杯右侧中逐滴加入适量浓盐酸或适量40% NaOH溶液,发现电流表指针都发生偏转。
+I2+H2O”设计成的原电池装置,其中C1、C2、C3、C4均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸或40% NaOH溶液,电流表指针都不发生偏转;乙组经思考后先添加了一种离子交换膜,然后向图Ⅱ烧杯右侧中逐滴加入适量浓盐酸或适量40% NaOH溶液,发现电流表指针都发生偏转。
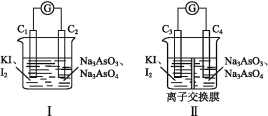
①甲组电流表指针都不发生偏转的原因是 。
②乙组添加的是 (填“阴”或“阳”)离子交换膜。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com