
����̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ���������̼����������Ϊ��ѧ���о�����Ҫ���⡣
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��(����ƽ���ϵ�����ں�����)
__ C+ __ KMnO4+ ___ H2SO4��___CO2��+ ___MnSO4 + ___K2SO4+ ___H2O?
����Ӧ����2��408��1024�����ӷ���ת��ʱ����ԭ��������Ϊ ????????????
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������������з�ӦCO��g����H2O��g�� CO2��g����H2��g�����õ���������������
CO2��g����H2��g�����õ���������������
ʵ���� | �¶��� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | x | 2��0 | 1��6 | 2��4 | 6 |
2 | 900 | 2��0 | 1��0 | 0��4 | 1��6 | 3 |
��ʵ��1����v(CO2����ʾ�ķ�Ӧ����Ϊ?? ???? ?? (Ҫ��2λ��Ч���֣���ͬ)��ʵ��2�ﵽƽ��ʱCO���������Ϊ?? ????? ???? ��
������Ӧ��ƽ�ⳣ������CO��Ч�ʸߣ�������÷�Ӧƽ�ⳣ���Ĵ�ʩ��????????? ��
��900��ʱ�����ܱ������У�����4 molCO��3 mol H2O ��4mol CO2��2��4mol H2���Ƚϴ�ʱ�����淴Ӧ���ʵĴ�С��v�� ______ v�� ��������������������������)��
��һ��������������Ӧ��ij����̶����ܱ������н��У���˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����?? ? ��?
A�������������ƽ������������ʱ����仯???
B������1molH2��ͬʱ����1molCO
C��������������ܶȲ���ʱ����仯?????????
D��CO2�������������ʱ����仯????
��3������β�����ŷŶԿ��������Ⱦ��Ŀǰ���õ�������������װ���а�װһ����������������Ч��β���е��к�����ת�����磺
�� CO (g)+NO2(g) ��CO2(g) + NO (g)?? ��H ����a kJ��mol?? (a��0)
��? 2CO (g)+2NO(g) ��2CO2(g) )+ N2 (g)?? ��H ����b kJ��mol? (b��0)
���ñ�״����3��36LCO��ԭNO2��N2(CO��ȫ��Ӧ)ʱ�ų�������Ϊ??? ??? kJ(�ú�a��b�Ĵ���ʽ��ʾ����ͬ)����д���÷�Ӧ���Ȼ�ѧ����ʽ???????????????????????????????? ��
��1��5��4��6��5��4��2��6?? ��2�֣���? 12g? ��2�֣�
��2���� 0��13 mol��L-l�� min-l��2������ 0�� 53��2����
�� �����¶ȣ�2����??? �� ����2����?? �� B D��2����
��3��? 3(2a+b)/80��2���� ��
4CO (g)+2NO2(g) ��4CO2(g) )+ N2 (g)? ��H��-(2a+b) kJ��mol ��2����
��������
�����������1�����ݻ��ϼ���������ƽ�÷�Ӧ�������������Ԫ�ػ��ϼ۽���5�ۣ�̼Ԫ�ػ��ϼ�����4�ۣ����ϼ����������ڻ��ϼ۽����������Ը������ǰ��ϵ����4��̼����ǰ��ϵ����5������ԭ���غ㣬��ƽ�������ʵ�ϵ������ƽ���£�5 C+ 4 KMnO4+ 6 H2SO4 �T 5CO2�� + 4MnSO4 + 2 K2SO4+ 6 H2O���÷�Ӧת�Ƶ�������20������Ӧ����2��408��1024�����ӷ���ת��ʱ����ԭ��̼��������Ϊm����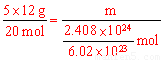 �����m=12 g ��
�����m=12 g ��
��2����ʵ��1���ﵽƽ��ʱ����CO2�����ʵ�������H2�����ʵ���Ϊ1��6mol������v(CO2)=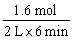 =0��13 mol��L-l�� min-l��
=0��13 mol��L-l�� min-l��
ʵ��2�ﵽƽ��ʱCO�������������ɸ������η����£�
CO(g)+H2O(g)  H2(g)+CO2(g)
H2(g)+CO2(g)
��ʼ��/mol? 2��0??? 1��0?????? 0???? 0??????????
ת����/mol? 0��4??? 0��4????? 0��4??? 0��4????????
ƽ����/mol? 1��6??? 0��6????? 0��4??? 0��4???????
ʵ��2�ﵽƽ��ʱCO���������Ϊ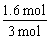 =0��53��
=0��53��
�ڸ������η������ͬ�¶��µ�ƽ�ⳣ����K(650��)= 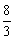 ��K(900��)=
��K(900��)= 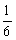 �������¶�ƽ�ⳣ����С����֪�����¶�ƽ�������ƶ����ָı�ѹǿ�Ը÷�Ӧƽ����Ӱ�죬��������÷�Ӧƽ�ⳣ���Ĵ�ʩֻ���ǽ����¶�ʹƽ�������ƶ���
�������¶�ƽ�ⳣ����С����֪�����¶�ƽ�������ƶ����ָı�ѹǿ�Ը÷�Ӧƽ����Ӱ�죬��������÷�Ӧƽ�ⳣ���Ĵ�ʩֻ���ǽ����¶�ʹƽ�������ƶ���
�۸������µ�Ũ�Ȼ�Qc=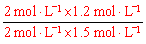 =0��8��K(900��)��ƽ�����淴Ӧ�����ƶ�����v�� ��v����
=0��8��K(900��)��ƽ�����淴Ӧ�����ƶ�����v�� ��v����
��A���÷�ӦΪ���巴Ӧ����Ӧǰ�������ʵ������䣬���������غ㣬���������ƽ������������ʱ����仯������B������1 mol H2��ͬʱ����1 mol CO�����������淴Ӧ������ȣ���ȷ��C���̶�������ܱ��������������䣬������䣬�����ܶ�Ҳ���ı䣬����D��CO2�������������ʱ����仯����ȷ��
��3�����ݸ�˹���ɣ���+�� 2�õ���
2�õ���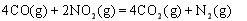 ��H=-(2a+b)kJ/mol ��3��36 L CO��ԭNO2��N2ʱ�ų�������Ϊ
��H=-(2a+b)kJ/mol ��3��36 L CO��ԭNO2��N2ʱ�ų�������Ϊ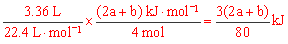 ��
��
������������ԭ��Ӧ����ƽ�ͼ��㣬��ѧ��Ӧ���ʼ��㣬ƽ��״̬��־���жϣ���ѧƽ��ļ��㣬��˹���ɵļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2013?����һģ������̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӣ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ����
��2013?����һģ������̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӣ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ����| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����̼ѭ������������ĸ߶����ӣ���֪ú������ȿ�����ˮ������Ӧ������CO��H2Ϊ���ĺϳ������ϳ����й㷺Ӧ�ã��Իش��������⣺
����̼ѭ������������ĸ߶����ӣ���֪ú������ȿ�����ˮ������Ӧ������CO��H2Ϊ���ĺϳ������ϳ����й㷺Ӧ�ã��Իش��������⣺| c(CO2) |
| c(CO) |
| 0.025mol/L |
| 0.1mol/L |
| c(CO2) |
| c(CO) |
| 0.025mol/L |
| 0.1mol/L |
| c(CH3OH) |
| c(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�������ʡ��Ȫһ�и�����һѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��16�֣�����̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ����
(1)�õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��(ϵ����˳�����ڴ������)
___ C+ ___ KMnO4+ ____ H2SO4��____CO2��+ ____MnSO4 + ____K2SO4+ ____H2O
(2)����ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ�������,���з�Ӧ
CO��g����H2O��g�� CO2��g����H2��g�����õ������������ݣ�
CO2��g����H2��g�����õ������������ݣ�
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1��6 | 2��4 | 6 |
| 2 | 900 | 2 | 1 | 0��4 | 1��6 | 3 |
| 3 | 900 | a | b | c | d | t |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�켪��ʡ��ͨ��ѧ������ѧ�����н�ѧ����������ۻ�ѧ���� ���ͣ������
����̼ѭ������������ĸ߶����ӣ���֪ú������ȿ�����ˮ������Ӧ������CO��H2Ϊ���ĺϳ������ϳ����й㷺Ӧ�á��Իش��������⣺
��1����¯������CO�������Ҫ��;֮һ���������ӦΪ��
FeO(s)��CO(g)  Fe(s)��CO2(g) ��H ��0
Fe(s)��CO2(g) ��H ��0
��֪��1100��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=0.263��
���¶����ߣ���ѧƽ���ƶ���ﵽ�µ�ƽ�⣬��ʱƽ�ⳣ��Kֵ__________�����������С�����䡱����
��1100��ʱ��ø�¯�У�c(CO2)=0.025mol��L-1��c(CO)="0.1" mol��L-1��������������£��÷�Ӧ��_______���У�����ҡ������ж�������
��
��2��һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����
��֪��2CO(g) + O2(g)��2CO2(g) ��H ���C566 kJ��mol�D1
2H2O(g) ��2H2(g) + O2(g) ��H ��+484 kJ��mol�D1
CH3OH(g) + 1/2O2(g)��CO2(g) + 2H2(g) ��H ���C192.9 kJ��mol�D1
��д��CO��H2��һ�������·�Ӧ����CH3OH(g)���Ȼ�ѧ����ʽ
��
��3��Ŀǰ��ҵ��Ҳ����CO2������ȼ�ϼ״����йط�ӦΪ��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H ��-49.0 kJ��mol-1���������Ϊ1 L���ܱ� �����У�����1mol CO2��3mo
CH3OH(g)+H2O(g) ��H ��-49.0 kJ��mol-1���������Ϊ1 L���ܱ� �����У�����1mol CO2��3mo l H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��
l H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��_______ _��
�ڷ�Ӧ�ﵽƽ������д�ʩ��ʹ �������______������ţ���
�������______������ţ���
| A�������¶� | B���ٳ���H2 | C���ٳ���CO2 |
| D����H2O(g)����ϵ�з��� E������He(g) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com