
(7分)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2983.2 kJ·mol-1①
P(s,红磷)+O2(g)===P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为__________________。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。
科目:高中化学 来源: 题型:
| 5 |
| 4 |
| 1 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
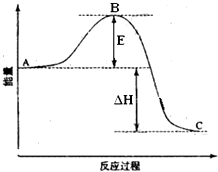 Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.
Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.| 5 |
| 4 |
| 1 |
| 4 |
查看答案和解析>>
科目:高中化学 来源:2009—2010学年衡水中学高二下学期期末考试化学 题型:填空题
(6分)填空:
(1)在测定硫酸铜结晶水含量实验过程中,称量操作至少进行 次。当加热到
时,停止加热,并将坩埚放在 中冷却。当 时则可认为结晶水已经完全失去。实际操作中,有些操作会使实验结果偏高或偏低。下列操作会使测定结果偏高的是 (填字母)
| A.加热温度过高而使硫酸铜部分分解 | B.坩埚用水洗后没有烘干 |
| C.加热后放在空气中冷却 | D.粉末未完全变白就停止加热 |
查看答案和解析>>
科目:高中化学 来源:2009-2010学年衡水中学高二下学期期末考试化学 题型:填空题
(6分)填空:
(1)在测定硫酸铜结晶水含量实验过程中,称量操作至少进行 次。当加热到
时,停止加热,并将坩埚放在 中冷却。当 时则可认为结晶水已经完全失去。实际操作中,有些操作会使实验结果偏高或偏低。下列操作会使测定结果偏高的是 (填字母)
A.加热温度过高而使硫酸铜部分分解 B.坩埚用水洗后没有烘干
C.加热后放在空气中冷却 D.粉末未完全变白就停止加热
(2)同素异形体相互转化的反应热相当小而且转化速度较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的观点“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”来研究。已知: P4(s、白磷)+5O2(g)=P4O10(s);△H=-2983.2kJ·mol-1
P(s、红磷)+5/4O2(g)=1/4P4O10(s);△H=-738.5kJ·mol-1
由此可知白磷的稳定性比红磷_____。(填写“强”或“弱”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com